
【题目】下列有关晶胞的叙述错误的是( )
A.晶胞是描述晶体结构的基本单元B.整块晶体中,相邻晶胞之间没有间隙
C.晶胞一般都是平行六面体D.晶胞都是正八面体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有三种有机物的分子式均为C8H8,其键线式分别表示为X:![]() ,Y:
,Y:![]() ,Z:
,Z:![]() 。下列说法正确的是
。下列说法正确的是
A. X、Z分子中所有原子一定在同一平面内
B. X、Y、Z都能发生取代反应、加成反应和氧化反应
C. X、Y、Z互为同分异构体,它们二氯代物的同分异构体数目不相同
D. X、Y、Z都能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号内的试剂除去下列各物质中少量的杂质,正确的是( )
A.溴苯中的溴(碘化钾溶液)
B.硝基苯中溶有二氧化氮(水)
C.乙烷中的乙烯(氢气)
D.苯中的甲苯(溴水)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500多年前,一艘载着天然苏打晶体的商船在航行中搁浅,船员们便在附近的沙滩上用几块苏打晶体支锅煮饭。之后他们惊奇地发现,锅下苏打在沙粒接触处出现了许多晶莹发亮的珠子。回答下列问题
(1)请你分析一下,这种珠子可能是_____________
A.水晶颗粒 B.无水碳酸钠 C.玻璃珠 D.晶体硅
(2)实验室可在坩埚中模拟制备此物质,下列坩埚中可选用的是_______(填字母)。
A.普通坩埚 B.石英坩埚 C.刚玉坩埚 D.铁坩埚
(3)制备此物质的主要反应方程式为_________(任写一个)。
(4)氢氟酸常用作此物质的蚀刻剂,原因为:_________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 如果严重缺Fe,可能会导致贫血
B. 组成蛋白质、核酸、糖类、脂质的共有元素是C、H、0、N、P
C. 越冬的植物细胞内,自由水/结合水的值下降
D. 细胞中的某些无机盐离子对维持细胞的酸碱平衡具有一定的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42﹣、CO32﹣ .
(1)为了进一步确认,对该溶液进行实验检测: 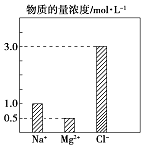
实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无 | 肯定无该离子的理由 |
步骤二 | 该溶液呈无色、透明、均一状态 | 肯定无 | 肯定无该离子的理由 |
步骤三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42﹣、H+;肯定无Ba2+ | 肯定有H+的理由 |
(2)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、、灼烧、在干燥器中冷却.
(3)原溶液中H+物质的量浓度为mol/L.
(4)向溶液中加入NaHCO3溶液,反应的离子方程式为: .
(5)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时加入的Ba(OH)2溶液体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

回答下列问题:
(1)过程I加NaOH溶液的作用是___________________________(用离子方程式表示);鼓入大量空气的目的是____________________________。
(2)已知:水体中以+l价或单质形式存在的氯元素,称为“余氯”。过程Ⅱ中加入适量液氯,控制pH在6-7,将氨氮转化为N2。实验测定氯铵比与余氯、残余NH4+的浓度关系如下图所示。

①为了完全从废水中去除氨氮,根据图像分析,投入的Cl2与NH4+的最佳比值为_________。
②过程Ⅱ分步发生3个反应:
i.Cl2+H2O =H++Cl- +HClO
ii.NH4++HClO==NH2Cl+H++H2O(NH2Cl中Cl元素为+l价)
iii.HClO继续参与反应,其离子方程式为________________________________。
③图中a点余氯浓度较大的原因是________________________________________。
(3)若含余氯废水中折合Cl2的含量是71 mg·L-1,则处理10m3含余氯废水,至少添加Na2SO3_____kg(溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3+、Fe2+、NH4+、H+、H2O、NO3-六种粒子,它们都是同一氧化还原反应中的反应物或生成物。下列叙述中不正确的是( )
A.该反应中氧化剂与还原剂的物质的量之比为1∶8
B.若有1mol NO3-发生还原反应,转移的电子数为8mol
C.该反应说明Fe(NO3)2溶液不宜加酸酸化
D.若把该反应设计成原电池,负极的反应为Fe2+-e-=Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com