
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、H+、SO42﹣、CO32﹣ .
(1)为了进一步确认,对该溶液进行实验检测: 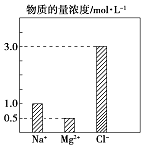
实验操作与现象 | 实验结论 | 判断理由 | |
步骤一 | 仔细观察坐标图 | 肯定无 | 肯定无该离子的理由 |
步骤二 | 该溶液呈无色、透明、均一状态 | 肯定无 | 肯定无该离子的理由 |
步骤三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42﹣、H+;肯定无Ba2+ | 肯定有H+的理由 |
(2)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、、灼烧、在干燥器中冷却.
(3)原溶液中H+物质的量浓度为mol/L.
(4)向溶液中加入NaHCO3溶液,反应的离子方程式为: .
(5)若向 100mL 该溶液中加入 1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时加入的Ba(OH)2溶液体积为L.
【答案】
(1)CO32﹣;碳酸根离子和镁离子之间会反应;Fe3+;该离子为黄色;电荷守恒
(2)洗涤
(3)1.2
(4)H++HCO3﹣=H2O+CO2↑
(5)0.1
【解析】解:溶液中含有镁离子,所以一定不含CO32﹣ , 根据电荷守恒,阳离子正电荷浓度总和:1mol/L+0.5×2mol/L=2mol/L,该溶液呈无色、透明、均一状态,一定不含Fe3+ , 加入足量BaCl2溶液,生成23.3g即0.1mol白色沉淀硫酸钡,再加稀硝酸,沉淀不消失,一定含有硫酸根0.1mol,一定不含钡离子,阴离子负电荷总浓度3mol/L+0.1mol/L×2=3.2mol/L,所以一定含有氢离子,浓度是1.2mol/L,所以答案是:CO32﹣;碳酸根离子和镁离子之间会反应;Fe3+;该离子为黄色;电荷守恒;(2)实验操作的步骤三中称量沉淀前的实验操作步骤有:过滤、洗涤、灼烧、在干燥器中冷却,所以答案是:洗涤;(3)原溶液中H+物质的量浓度为1.2mol/L,所以答案是:1.2;(4)溶液中含有氢离子,向溶液中加入NaHCO3溶液,反应的离子方程式为:H++HCO3﹣=H2O+CO2↑,所以答案是:H++HCO3﹣=H2O+CO2↑;(5)向100mL 该溶液中含有硫酸根0.1mol,向100mL该溶液中加入1mol/L 的 Ba(OH)2溶液,恰好沉淀完全时,加入的Ba(OH)2溶液物质的量是0.1mol,体积是 ![]() =0.1L,所以答案是:0.1.
=0.1L,所以答案是:0.1.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】香草醛用作化妆品的香精和定香剂,也是食品香料和调味剂,还可做抗癲痫药。香草醛的分子结构如图,下列关于香草醛的说法中,不正确的是( )

A. 该化合物的分子式为C8H6O3
B. 遇FeCl3溶液会显紫色
C. 最多能与4 mol H2发生加成反应
D. 与香草醛有相同官能团且苯环上有三个取代基的香草醛的同分异构体(包括香草醛)有10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成.电池的总反应式为2CH3OH+3O2+4OH-═2CO32-+6H2O.则下列说法正确的是
A. 电池放电时通入空气的电极为负极
B. 由于CO32-水解显碱性,电池放电时,电解质溶液的pH逐渐增大
C. 电池放电时负极的电极反应式为CH3OH+8OH--6e-═CO32-+6H2O
D. 电池放电时每消耗1 mol CH3OH转移8 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶胞的叙述错误的是( )
A.晶胞是描述晶体结构的基本单元B.整块晶体中,相邻晶胞之间没有间隙
C.晶胞一般都是平行六面体D.晶胞都是正八面体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷是第ⅤA族元素,黄砷(As4)是砷元素的一种单质,其分子结构与白磷(P4)相似。下列关于黄砷和白磷的叙述正确的是()
A.黄砷和白磷分子中共价键的键角均为109.5o
B.黄砷分子中共价键的键能大于白磷分子
C.黄砷分子的极性大于白磷分子
D.黄砷的熔点高于白磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的联接并填空:

(1)在A图中,使铜片上冒H2气泡。请加以必要联接__________(在答题卡的图中画线),则联接后的装置叫_________。电极反应式:锌板:____________________;铜板:___________。
(2)在B图中(a、b均为惰性电极),使a极析出铜,则b析出____________。加以必要的联接后,该装置叫___________。电极反应式:a极:___________________________b极:____________________________。经过一段时间后,停止反应并搅均溶液,溶液的pH值________________(升高、降低、不变),加入一定量的____________后,溶液能恢复至与电解前完全一致。
(3)工业上利用甲烷和氧气直接氧化制取甲醇的反应如下:
CH4+![]() O2(g) ==== CH3OH(g) △H=-128.5kJ/mol
O2(g) ==== CH3OH(g) △H=-128.5kJ/mol
副反应有:CH4(g)+![]() O2(g) ==== CO(g)+2H2O(g) △H=a kJ/mol
O2(g) ==== CO(g)+2H2O(g) △H=a kJ/mol
CH4(g)+2O2(g) ==== CO2(g)+2H2O(g) △H=b kJ/mol
CH4(g)+O2(g) ==== HCHO(g) +H2O(g) △H=c kJ/mol
甲醇与氧气反应生成HCHO(g)和水蒸汽的热化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是
A. 金属Mg与稀硫酸、CO2均能反应,但其基本反应类型不同
B. 浓硫酸与铜反应时,既体现了其强氧化性又体现了其酸性
C. 铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
D. SO2气体通入Ba(NO3)2溶液中,有白色沉淀生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com