
 Ag+(aq)+Cl-(aq)在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为 (填序号),此时溶液②中Cl-物质的量浓度为 。
Ag+(aq)+Cl-(aq)在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 mL蒸馏水 ②100 mL 0.3 mol·L-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为 (填序号),此时溶液②中Cl-物质的量浓度为 。 H++CO32-;HCO3-+H2O
H++CO32-;HCO3-+H2O H2CO3+OH-; H2O
H2CO3+OH-; H2O H++OH-
H++OH-  H++OH- ;NH4+发生水解反应消耗OH-,H2O+ NH4+
H++OH- ;NH4+发生水解反应消耗OH-,H2O+ NH4+ NH3·H2O + OH-,所以c(H+)>c(OH-)。盐的电离作用大于弱电解质水的电离,所以c(SO42-)>c(H+)。因此在该溶液中离子浓度由大到小的顺序为c(NH4+)>c(SO42-)>c(H+)>c(OH-)。(2)NaHCO3在该溶液中存在的平衡有电离平衡HCO3-
NH3·H2O + OH-,所以c(H+)>c(OH-)。盐的电离作用大于弱电解质水的电离,所以c(SO42-)>c(H+)。因此在该溶液中离子浓度由大到小的顺序为c(NH4+)>c(SO42-)>c(H+)>c(OH-)。(2)NaHCO3在该溶液中存在的平衡有电离平衡HCO3- H++CO32-;H2O
H++CO32-;H2O H++OH- ;和水解平衡HCO3-+H2O
H++OH- ;和水解平衡HCO3-+H2O H2CO3+OH-。(3)某温度时,0.01mol/L的NaOH溶液,c(OH-)=10-2mol/L,c(H+)=10-11mol/L.由于c(H+)·c(OH-)=10-13>10-14=Kw,则该温度高于25℃。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10 mol/L,则说明水的电离受到了抑制。若外加酸,则c(H+)(酸)=10-3mol/L,该溶液的pH为3;若外加碱,则c(H+)1×10-10 mol/L.pH="10." 即该溶液的pH为3或10. (4)由于醋酸是弱酸,部分电离;NaOH是强碱,全部电离。当二者电离产生的离子浓度相等时,酸的浓度远大于碱的浓度。当二者溶液等体积混合时由于酸过量,中和后未电离的酸分子会继续电离。所以混合后溶液呈酸性。此时溶液中c(Na+)<c(CH3COO-)。(5)若物质的量浓度相同的CH3COOH和NaOH溶液混合后,溶液中醋酸根离子和钠离子浓度相等。根据电荷守恒可得:c(Na+)+ c(H+)=c(OH-)+c(CH3COO-),所以c(H+)=c(OH-)。溶液显中性。由于醋酸是弱酸,部分电离,而NaOH是强碱完全电离。所以醋酸体积>氢氧化钠溶液体积。(6)向含有足量AgCl固体的饱和溶液加入①100 mL蒸馏水,会使测定溶解平衡AgCl(s)
H2CO3+OH-。(3)某温度时,0.01mol/L的NaOH溶液,c(OH-)=10-2mol/L,c(H+)=10-11mol/L.由于c(H+)·c(OH-)=10-13>10-14=Kw,则该温度高于25℃。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10 mol/L,则说明水的电离受到了抑制。若外加酸,则c(H+)(酸)=10-3mol/L,该溶液的pH为3;若外加碱,则c(H+)1×10-10 mol/L.pH="10." 即该溶液的pH为3或10. (4)由于醋酸是弱酸,部分电离;NaOH是强碱,全部电离。当二者电离产生的离子浓度相等时,酸的浓度远大于碱的浓度。当二者溶液等体积混合时由于酸过量,中和后未电离的酸分子会继续电离。所以混合后溶液呈酸性。此时溶液中c(Na+)<c(CH3COO-)。(5)若物质的量浓度相同的CH3COOH和NaOH溶液混合后,溶液中醋酸根离子和钠离子浓度相等。根据电荷守恒可得:c(Na+)+ c(H+)=c(OH-)+c(CH3COO-),所以c(H+)=c(OH-)。溶液显中性。由于醋酸是弱酸,部分电离,而NaOH是强碱完全电离。所以醋酸体积>氢氧化钠溶液体积。(6)向含有足量AgCl固体的饱和溶液加入①100 mL蒸馏水,会使测定溶解平衡AgCl(s) Ag+(aq)+Cl-(aq)正向移动,直至达到新条件下的平衡状态。由于在25℃时,AgCl的Ksp=1.8×10-10,所以c2(Ag+)= 1.8×10-10, c(Ag+)= 1.34×10-5mol/L. ②100 mL 0.3 mol·L-1 AgNO3溶液中, c(Ag+)=" 0.3" mol/L; ③100 mL 0.1 mol·L-1MgCl2溶液,c(Cl-)="0.2mol/L," c(Ag+)= 1.8×10-10÷0.2=9×10-10.所以充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为②①③。此时溶液②中Cl-物质的量浓度为1.8×10-10÷0.3=6×10-10mol/L.
Ag+(aq)+Cl-(aq)正向移动,直至达到新条件下的平衡状态。由于在25℃时,AgCl的Ksp=1.8×10-10,所以c2(Ag+)= 1.8×10-10, c(Ag+)= 1.34×10-5mol/L. ②100 mL 0.3 mol·L-1 AgNO3溶液中, c(Ag+)=" 0.3" mol/L; ③100 mL 0.1 mol·L-1MgCl2溶液,c(Cl-)="0.2mol/L," c(Ag+)= 1.8×10-10÷0.2=9×10-10.所以充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为②①③。此时溶液②中Cl-物质的量浓度为1.8×10-10÷0.3=6×10-10mol/L.

科目:高中化学 来源:不详 题型:填空题
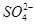 、
、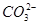 、
、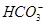 、
、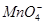 。
。 。
。| 实验操作 | 现象 |
| a.取少量粉末,加水、振荡 | 全部溶解、 |
| 溶液无色透明 | |
| b.向所得溶液中慢慢滴入苛性钠溶液,并加热 | 无明显现象 |
| c.取少量粉末,加盐酸 | 无明显现象 |
| d.取少量粉末,加稀H2SO4和稀HNO3的混合液 | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol/LNa2CO3溶液:c(OH-)= 2c(H2CO3)+ c(HCO3-)+ c(H+) |
| B.能使紫色石蕊试液呈红色的溶液:Na+、NH、I-、NO可以大量共存 |
| C.任何条件下,pH=13的氢氧化钠溶液中:c(OH-)=0.1mol/L |
| D.NH4HCO3溶于过量的NaOH溶液中:HCO3-+ OH-= CO32- + H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使酚酞变红色的溶液:Fe3+、Mg2+、SO42-、NO3- |
| B.KNO3的酸性溶液:Fe2+、Ca2+、Al3+、Cl- |
| C.常温下,由水电离出的c(H+)=1.0×10-10 mol·L-1的溶液:NH4+、Na+、SiO32-、CO32- |
| D.透明的溶液:Cu2+、Fe3+、NO3-、MnO4- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0 mol·L-1的KNO3溶液中:H+、Fe2+、Cl-、SO42- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.能使pH试纸变红的溶液中:K+、Ba2+、AlO2-、Cl- |
| D.pH=0的溶液中:Mg2+、Na+、F-、SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实 验 | 解释 |
| A | 100℃ 0.1 mol/LNa2SO4溶液pH= 6.2 | H2O H+ + OH- H+ + OH- |
| B | 0.1 mol/L CH3COOH的pH=3 | CH3COOH CH3COO- + H+ CH3COO- + H+ |
| C | 配制FeCl3溶液时加少量盐酸 | Fe3+ + 3OH- Fe(OH)3 Fe(OH)3 |
| D | 用稀硫酸洗涤BaSO4,沉淀损失小 | BaSO4(s)  Ba2+(aq) + SO42-(aq) Ba2+(aq) + SO42-(aq) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al3+、CO32-、Cl- | B.Na+、NH4+、Cl- |
| C.Mg2+、Cl-、Fe2+ | D.Mg2+、Ba2+、Br- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同物质的量浓度的下列溶液:①NH4Al(SO4)2、②NH4C1、③CH3COONH4、④NH3·H2O,c(NH4+)由大到小的顺序是:①>②>③>④ |
| B.某溶液中由水电离出的c( H+)=1×l0-amol/L,若a>7时,则该溶液的pH一定为14-a |
| C.常温下,向AgCl悬浊液中加入少量NaC1固体后振荡,c(Cl-)增大,Ksp(AgCl)增大 |
| D.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c(R2-) +c(HR-)=c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com