
【题目】下列说法中,正确的是
A. 物质的化学反应与体系的能量变化不是同时发生的
B. 化学键可以使离子相结合,不可以使原子相结合
C. 相同温度、压强时,等体积的O2和O3含有相同数目的原子
D. 在周期表中金属与非金属分界处,可以找到半导体材料
科目:高中化学 来源: 题型:
【题目】在水溶液中能大量共存的一组离子是
A.Na+、Al3+、Cl-、CO32-
B.Ca2+、Al3+、Br-、CO32-
C.K+、Ca2+、Cl-、NO3-
D.K+、NH4+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
化学式 | AgCl | Ag2CrO4 | CH3COOH | HC1O | H2CO3 |
KSp 或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10 -5 | Ka=3.0×10-8 | Ka1=4.1×10一7 Ka =5.6×10-11 |
A.相同浓度CH3COONa和Na2CO3的混合液中,各离子浓度的关系有:
c(Na+ )>c(CO32- )>c(CH3COO一)>c(OH-)>c(H+)
B.向0.1 mol/LCH3COOH溶液中滴加NaOH溶液至溶液pH=5,此时 c(CH3COO) : c(CH3COO 一)=9 : 5
C.少量碳酸氢钠固体加入到新制的氯水中,c(HClO)增大
D.向浓度均为1×10-3mol/L的KC1和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中放入1L气体R和3L气体Q,在一定条件下发生反应
R(g)+3Q(g)=X(g)+nY(g),反应完全后,容器温度不变,混合气体的压强是原来的75%,则化学方程式中n的值是 ( )
A.2B.3C.4D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下反应方程式:
A.CuO+H2![]() Cu+H2O B.2KClO3
Cu+H2O B.2KClO3![]() 2KCl + 3O2↑
2KCl + 3O2↑
C.Cl2+2NaOH==NaCl + NaClO+ H2O D.2FeBr2 + 3Cl2=2FeCl3+ 2Br2
E.MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O G.KClO3+6HCl(浓)==KC1+ 3H2O + 3Cl2↑
MnCl2+Cl2↑+2H2O G.KClO3+6HCl(浓)==KC1+ 3H2O + 3Cl2↑
H.HgS +O2=Hg + SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原____________________
(2)同一种物质中,同种元素间发生氧化还原反应________________
(3)所有元素均参加氧化还原反应的是____________________________
(4)发生在不同物质间,只有部分元素被氧化或只有部分元素被还原的反应_______________
II.已知力程式G: KClO3+ 6HCI(浓)=KCl + 3H2O+ 3Cl2↑
(1)请用双线桥法标出电子转移的方向和数目_______________________
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是_________________________
(3)上述反应中氧化产物和还原产物的质量比为____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸(HClO2)是一种中强酸,易分解,亚氯酸及其盐类在工业生产和环境治理等方面用途非常广泛。回答下列问题:
(1)HClO2中氯元素的化合价为_______;亚氯酸不稳定,易分解为Cl2、ClO2和H2O,分解后的氧化产物与还原产物的物质的量之比为__________________。
(2)已知常温下Ka(HClO2)=1.1×10-2,则反应HClO2+OH-![]() ClO2-+H2O在常温下的平衡常数K=_________________。
ClO2-+H2O在常温下的平衡常数K=_________________。
(3)亚氯酸盐可用于脱除氮氧化物和硫氧化物,当其他条件不变时,测得脱除率与吸收液pH的关系如图所示。已知:C12和ClO2溶于水后更易与SO2和NO反应。

①亚氯酸盐脱除SO2的离子方程式为________________________。
②pH越小,脱除率越大,其原因是____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某同学欲配制100 mL 0.10 mol·L-1的CuSO4溶液。以下操作1~5是其配制的过程及示意图:
操作1:准确称取一定质量的胆矾晶体并用适量蒸馏水溶解。
操作2:将所得溶液转移到仪器X中,用蒸馏水冲洗烧杯和玻璃棒2~3次,将洗涤液也转移到X中。
操作3:继续向X中加蒸馏水至液面离X的刻度线1~2 cm处。
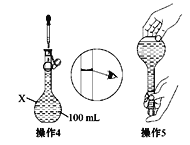
①仪器X的名称是________。称量过程中主要用到的仪器是_____________。在将烧杯中的溶液转移至容量瓶中,为了防止溶液溅出,应采取什么措施____________________。
②关于该配制过程,下列说法正确的是________。
A.操作1中,应称取胆矾晶体的质量为2.5 g
B.操作2中,洗涤液不需要转移到仪器X中
C.操作4称为定容,由于该同学的观察方法不正确,将导致所配溶液浓度偏低
D.操作5摇匀后静置,发现液面低于刻度线,应继续加水至凹液面与刻度线相切
(2)为实现金属钠在隔绝空气条件下与水反应并收集生成的气体,某研究性学习小组设计了如图发生装置。

① Y液体可以选用________。
A.煤油 B.饱和的食盐水 C.四氯化碳
②实验前检验该装置气密性的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长时间运动引起机体缺氧时,血液pH的变化趋势、引起pH变化的物质、能起缓冲作用的物质分别是
A. 降低、CO2、H2CO3 B. 降低、乳酸、HCO3-
C. 升高、CO2、H2CO3 D. 升高、乳酸、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 能自发进行的反应都是放热反应
B. 凡是熵增加的反应一定能自发进行
C. 在一定条件下,吸热反应可以自发进行
D. 放热的熵增加的反应不一定能够自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com