
【题目】恒温恒容条件下发生反应:2NO2(g)![]() N2O4(g),下列叙述能够标志该反应达到化学平衡状态的有
N2O4(g),下列叙述能够标志该反应达到化学平衡状态的有
①体系的压强不再改变 ②气体的颜色不再改变
③气体的平均摩尔质量不再改变 ④混合气体的密度不再改变
⑤各组分的体积分数不再改变 ⑥原子总数不再改变
⑦混合气体分子总数不再改变 ⑧c(NO2):c(N2O4)=2:1,且比值不再改变
⑨v(NO2)正=2v(N2O4)逆
A.①②③⑤⑦⑧⑨B.②③⑤⑦⑨C.④⑤⑥⑦D.全部
【答案】A
【解析】
①体系的压强不再改变,由于是恒容的容器,可以判断反应达到平衡,①正确;
②气体的颜色不再改变,说明二氧化氮浓度不再变化,可以判断反应达到平衡,②正确;
③气体的平均摩尔质量不再改变,根据![]() 得,n减小,m不变,所以M始终在变化,当变化的量不变时,可以判断反应达到平衡,③正确;
得,n减小,m不变,所以M始终在变化,当变化的量不变时,可以判断反应达到平衡,③正确;
④混合气体的密度不再改变,根据![]() 得,V不变,m不变,所以密度始终不变,④错误;
得,V不变,m不变,所以密度始终不变,④错误;
⑤各组分的体积分数不再改变,可以判断反应达到平衡,⑤正确;
⑥原子总数始终不再改变,不可以判断反应达到平衡,⑥错误;
⑦分子总数一直在变化,所以当混合气体分子总数不再改变时,可以判断反应达到平衡,⑦正确;
⑧浓度一直在改变,所以当c(NO2):c(N2O4)=2:1,且比值不再改变时,可以判断反应达到平衡,⑧正确;
⑨化学反应达到平衡时,正反应速率和逆反应速率相等,所以当v(NO2)正=2v(N2O4)逆时,可以判断反应达到平衡,⑨正确;
答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质的检验说法不正确的是( )
A.加入氯化钡溶液有白色沉淀生成,再加稀硝酸沉淀不消失,一定含有![]()
B.观察钾元素焰色反应的操作是:将铂丝用稀盐酸洗涤后灼烧至火焰为无色,然后再用铂丝蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察
C.待检液加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有![]()
D.待检液加入氯化钡溶液有白色沉淀生成,再加入足量盐酸沉淀消失且产生无色无味的气体,则待检液中一定含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能正确表示下列变化的离子方程式是
A.用醋酸除去水垢:
B.用氢氧化钠溶液除去镁粉中的杂质铝:
C.室温下,测得小苏打溶液pH>7,证明碳酸是弱酸:![]()
D.将![]() 溶液与0.40mol·L-1NaOH溶液等体积混合:
溶液与0.40mol·L-1NaOH溶液等体积混合:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应的能量变化如图所示。下列说法正确的是

A.在通常状况下,金刚石比石墨更稳定
B.石墨的燃烧热为![]()
C.
![]()
D.12g石墨在一定量的空气中燃烧,生成气体产物36g,该过程放出的热量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]() ;将汽车尾气中的CO和NO气体转化CO2和N2是减少汽车尾气的有效途径之一,若用
;将汽车尾气中的CO和NO气体转化CO2和N2是减少汽车尾气的有效途径之一,若用![]() 、
、![]() 、
、![]() 、
、![]() 分别表示CO、NO、CO2、N2,在固体催化剂表面,上述反应的过程可用图表示,下列说法正确的是
分别表示CO、NO、CO2、N2,在固体催化剂表面,上述反应的过程可用图表示,下列说法正确的是

A.从吸附到解吸的过程中,能量状态最低的是C处
B.图示过程中,反应物断键吸收能量大于生成物形成所释放的能量
C.该反应的反应物浓度越大,反应速率一定越快
D.该反应中的固体催化剂起到反应载体的作用,未影响反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在人类的生产和生活中有着广泛的应用,某化学兴趣小组利用图一装置探究氨气的有关性质。
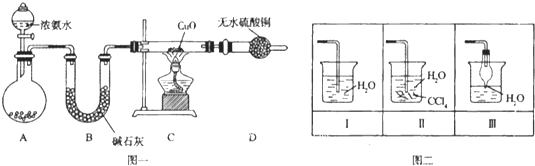
(1)装置A中烧瓶内试剂可选用 (填序号)。B的作用是
a.碱石灰 b.浓硫酸 c.生石灰 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 ,.该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑色固体A加热至红热投入到无色溶液B中发生如图转化关系。

(1)由此可以推断:A为________(填化学式,下同),B为_______,X为_______,C为_________,E为_________。
(2)写出A与B反应的化学方程式: ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以芳香族化合物A为主要原料,按下列线路合成抗癫痫药物W:

已知:![]()
请回答:
(1)下列说法正确的是________。
A.反应②是氧化反应 B.试剂X是浓硝酸和浓硫酸
C.反应③⑤的目的是保护![]() D.药物W的分子式是
D.药物W的分子式是![]()
(2)写出化合物C的结构简式________。
(3)写出反应⑥的化学方程式________。
(4)设计从G到H的合成路线(用流程图表示,无机试剂任选)________。
(5)写出化合物A的相邻同系物Y的同分异构体结构简式,且必须符合下列条件:________。
①能发生银镜反应;
②![]() 表明,分子中共有4种H原子;
表明,分子中共有4种H原子;
③除了苯环无其它环。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国平原地区地下水质量差,铁、锰含量较高,需进行处理才能达到饮用水标准。地下水中铁锰的来源主要是矿物FeCO3和MnCO3。
(1)酸雨地区地下水中铁含量更高,结合化学用语从平衡移动角度解释原因_______。
(2)去除Fe2+
①除铁滤池经过曝气3~7天后,滤料表面形成______色物质,其成分是Fe(OH)3,使得溶液中Fe2+含量迅速下降,其作用过程如图所示。
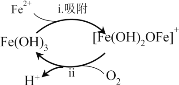
②将过程ii的离子方程式补充完整:________。
过程i:Fe2++Fe(OH)3=[Fe(OH)2OFe]++H+
过程ii:4[Fe(OH)2OFe]++ +10H2O= +
③有利于提高过程ii反应速率的措施是______(填序号)。
A. 降低温度 B. 通入足量O2 C. 搅拌
(3)去除Mn2+
向除锰滤池中加入ClO2将Mn2+氧化为MnO2,随着反应进行,滤池溶液的pH___(填“变大”“变小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com