
Ϊ֤��ij������һԪ�ᣨHX�������ᣬͬѧ�����������ʵ�鷽������������������
A�������£���0.1mol/L HX��Һ��pH ����pH��1��֤��HX������
B�������£���1mol/L NaX��Һ��pH ����pH��7��֤��HX������
C������Ũ�ȡ������HCl��NaX��Һ��ϣ��������ҺpH��7��֤��HX������
D������ͬ�����£���0.1 mol/L�������0.1mol/L��HX��Һ���е�����ʵ�飬������Ƚ�HX��Һ������Խϰ���֤��HXΪ����
 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��A��B��C���ֱ��ʹ��Ļ�����Ϊ���ȷݣ�һ�ݸ����������Ʒ�Ӧ�������� �� mol H2����һ����ȫȼ�պ����� 2�� mol CO2����û�ϴ��в����ܺ��� �� ��
A���״� B���Ҵ� C���Ҷ��� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ˵��HNO2Ϊ������ʵ��ǣ�
��0.1 mol/L HNO2��Һ��pH��2.1 �ڳ�����NaNO2��Һ��pH>7
����HNO2��Һ������ʵ��ʱ�����ݺܰ� ��HNO2��Һ��KCl��Һ��������Ӧ
��HNO2����̼���Ʒ�Ӧ��CO2 ��HNO2���ȶ����ֽ�
A���٢ڢۢݡ�������B���٢ڢܢ� C���٢ڢ� D���٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��CO��H2���Ժϳɶ����ѣ���ѧ����ʽΪ3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) ��H��0�� ���������Ӧ����ʽ��ƽ�ⳣ��Kֵ�����÷�Ӧ_ ��ѡ���ţ���
CH3OCH3(g)+CO2(g) ��H��0�� ���������Ӧ����ʽ��ƽ�ⳣ��Kֵ�����÷�Ӧ_ ��ѡ���ţ���
A��һ��������Ӧ�����ƶ� B����ƽ���ƶ�ʱ����Ӧ������������С
C��һ�����淴Ӧ�����ƶ� D����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
��2��һ�������£�������CO2(g)��H2(g)�ϳ�CH4(g)��ͬʱ������H2O(g)��
�� ��һ�ݻ�Ϊ2L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ��10min�ﵽƽ��ʱ�������ʵ�Ũ������ͼ1��ʾ��
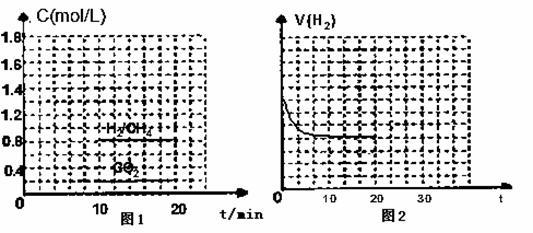
��CH4��ʾ�ﵽƽ��ʱ�ķ�Ӧ���� �����¶��µĵ�ƽ�ⳣ������ ��
�� ͼ2��ʾH2�ڽ���ƽ������е�����ʱ��ͼ��������20minʱ�����������������30minʱ�ִﵽ״̬������ͼ2�л���H2���淴Ӧ��������ʱ��ͼ��
��3�����������Ʒ�Ӧ2CO=2C+O2����H>0��������CO����Ⱦ�����жϸ÷�Ӧ�ܷ��Է�
����ܡ����ܡ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й��ڻ�ѧѧϰ���о���˵���������
A����ѧģ�������ڽ���һЩ��ѧ���� B�������غ㶨���Ǵ���ʵ����ʵ���ܽ�
C����ѧ������ļ��趼�ܱ�ʵ��֤ʵ D����ѧ����ԭ����Ӧ������һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ�г���������ͼ����ʾij�ֱ仯���̣��磺
��ƽ���ƶ����� ���к͵ζ�����
�۳��������ɺ��ܽ� �ܹ������ʵ��ܽ�ȱ仯����
��������ͼ�д��������α�ʾ���������е�
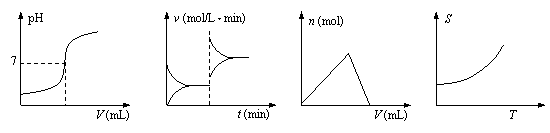

A. �٢ڢۢ� B. �ڢۢ٢� C. �ܢۢڢ� D. �ڢ٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ԫ�����ڱ���ӳ��Ԫ�����ʵ������Ա仯���ɡ������Ԫ�����ʼ������Ϣ�ش��������⣺
���������߷ֱ��ʾԪ�ص�ij��������˵�����Ĺ�ϵ��ZΪ�˵������YΪԪ�ص��й����ʣ�����������Ԫ���й�������������߱��������Ӧ�Ŀո��У�
�٢�A��Ԫ�ص���������ϼ� ��
�ڵ�����������Ԫ�ص�����������Ӧˮ����ļ��� ��
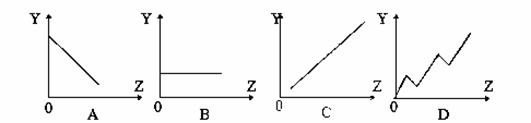
��ijͬѧ�õ������йؼ��ֶ�����Ԫ����Ϣ�ı���
��һ
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6����2 | +2 | ��2 |
����
| Ԫ�ش��� | Ԫ��������Ϣ |
| A | �䵥�����ܶ���С�����ʡ� |
| B | �����Ӵ�������λ����ɣ������ǿ�������Ҫ�ɷ�֮һ�� |
| C | ����������B������������ͬ�ĵ��Ӳ�ṹ������BԪ�ؿ����γ��������ϵ����ӻ���� |
| D | ����������������ﶼ�����ԣ���Cͬ���� |
| E | ��Cͬ���ڣ�ԭ�Ӱ뾶�ڸ�������С |
���������ű����У�ָ����ͬ��Ԫ�ص���__________________________������Ԫ�ش��ţ�
�������ű����У��ǽ�������ǿ��Ԫ��ԭ�ӵĵ����Ų�ʽΪ ����������ǿ��Ԫ��λ�����ڱ��ĵ� ���� �塣
��д��A��B��C�γɵĻ�����ĵ���ʽ
���ڶ���������Ԫ���У�EԪ�ؼ���������Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳����
(��Ԫ�ط��ű�ʾ)��
��QT2�γɵĻ������ڹ�̬ʱΪ_________���塣
����д��һ����˵��D��L������ǿ������ʵ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͬ��ͬѹ�£����и����Ȼ�ѧ����ʽ�У���H2>��H1���� �� �� A ��2H2(g) + O2(g)�� 2H2O(g) ��H1 �� 2H2(g) + O2(g) �� 2H2O(l) ��H2
B��S(g) + O2(g) ��SO2(g) ��H1 �� S(s) + O2(g) �� SO2(g) ��H2
C��CO(g) + 1/2 O2(g) = CO2(g) ��H1 ��2CO(g) + O2(g) = 2CO2(g) ��H2
D��C(s)+H2O(g)=CO(g)+H2(g) ��H1 ��CaO(s)��H2O(l)===Ca(OH)2(s)����H2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com