
已知298 K时下列物质的溶度积(单位略)。
| CH3COOAg | AgCl | Ag2CrO4 | Ag2S | |
| Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
下列说法正确的是( )
A.等体积、浓度均为0.02 mol·L-1的CH3COONa和AgNO3溶液混合能产生沉淀
B.向含有浓度均为0.01 mol·L-1的CrO 和Cl-的溶液中慢慢滴入AgNO3溶液时,CrO
和Cl-的溶液中慢慢滴入AgNO3溶液时,CrO 先沉淀
先沉淀
C.在CH3COOAg悬浊液中加入盐酸时发生反应的离子方程式为CH3COOAg+H++Cl-===CH3COOH+AgCl
D.298 K时,上述四种饱和溶液的物质的量浓度:
c(CH3COOAg)>c(AgCl)>c(Ag2CrO4)>c(Ag2S)
科目:高中化学 来源: 题型:
下列事实能说明影响化学反应速率的决定因素是反应物本身性质的是( )
A.Cu能与浓硝酸反应,而不能与浓盐酸反应
B.Cu与浓硝酸反应比与稀硝酸反应快
C.N2与O2在常温常压下不能反应,放电时可反应
D.Cu与浓硫酸能反应,而与稀硫酸不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组化合物的性质比较,不正确的是( )。
A.酸性:HClO4>HBrO4>HIO4 B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S>HCl D.非金属性:F>O>S
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是( )
A. 将Cl2通入溴化亚铁溶液:2Br-+Cl2===Br2+2Cl-
B. 用稀硫酸吸收氨气:NH3+H+===NH
C. AlCl3溶液中加入过量的氨水:Al3++4NH3·H2O=== AlO2-+4NH
D. 碳酸氢钠和稀硫酸反应:CO +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.pH=4的溶液中水电离出的H+一定是1×10-4mol/L
B.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成
D.AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B.合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
D.对于2HI(g) H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g) 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1 ②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1 ③平衡时物质A与B的转化率相等 ④平衡时物质B的浓度为0.2 mol·L-1 ⑤其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A.①②③ B.①③⑤ C.②④⑤ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
 结构为 的有机物可以通过不同的反应得到下列四种物质:
结构为 的有机物可以通过不同的反应得到下列四种物质:
 ① ②
① ②

 ③ ④
③ ④
生成这四种有机物的反应类型依次为
A.酯化、取代、缩聚、取代 B.取代、取代、加聚、消去
C.取代、缩聚、酯化、消去 D.取代、加成、酯化、消去
查看答案和解析>>
科目:高中化学 来源: 题型:
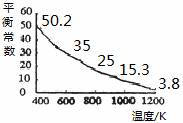
碘单质难溶于水却易溶于KI溶液。碘水中加入KI溶液发生反应:
I2(aq)+I-(aq)  I3-(aq),该反应的平衡常数与温度的关系如右图,下列说法不正确的是
I3-(aq),该反应的平衡常数与温度的关系如右图,下列说法不正确的是
A.上述正反应为放热反应
B.上述体系中加入苯,平衡不移动
C.可运用该反应原理除去硫粉中少量的碘单质
D.实验室配制碘水时,为增大碘单质的溶解度可加入适量KI溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com