



 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.电解法精炼粗铜,用纯铜作阴极 |
| B.电解熔融的氯化钠制取金属钠,用铁作阳极 |
| C.在镀件上电镀锌,用锌作阳极 |
| D.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
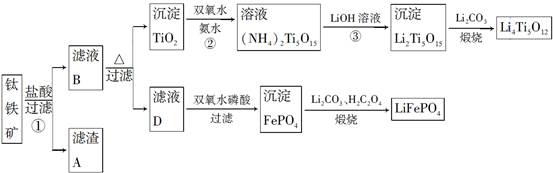
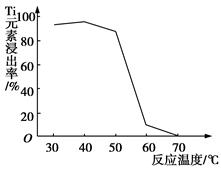
 Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。
Li7Ti5O12+3FePO4,该电池充电时阳极反应式是____________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
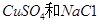 的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是
的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是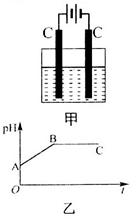
A.是该混合溶液中的 导致了A点溶液的pH值小于B点 导致了A点溶液的pH值小于B点 |
B.AB线段与BC线段在阴极上发生的反应是相同的即: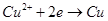 |
| C.BC段阴极产物和阳极产物的体积之比为2:1 |
| D.在整个电解的过程中会出现少量淡蓝色的Cu(OH)2沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
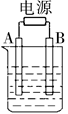
| A.图中B极同电源正极相连 |
| B.该蓝色溶液可能是Cu(NO3)2或CuCl2溶液[ |
| C.电解后溶液的pH约为 1(溶液体积变化忽略不计) |
| D.要使电解后溶液恢复到电解前的状态,则可加入2 g CuO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
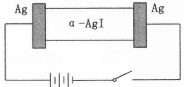
| A.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| B.若α-AgI是Ag+导电,则通电一段时间后晶体质量减少 |
| C.阳极反应为:Ag一e—=Ag+ |
| D.阴极质量不断增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a极发生还原反应 |
| B.每生成6.4 g Cu,转移电子0.2 mol |
C.阳极反应式: |
| D.在直流电源中电流从b流向a |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
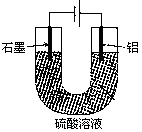
| A.阳极电极方程式为: Al—3e—+6OH—=Al2O3+H2O |
| B.随着电解的进行,溶液的pH逐渐增大 |
| C.当阴极生成气体3.36L(标况)时,阳极增重2.4g |
| D.电解过程中H+移向Al电极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
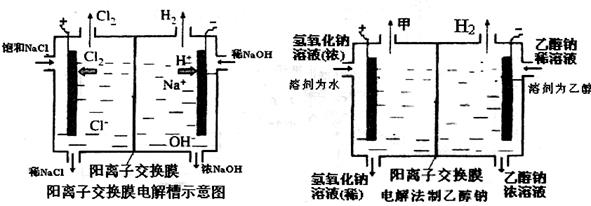
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com