
【题目】关于如图所示装置的叙述错误的是
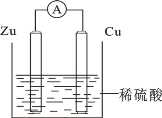
A. 锌是负极,其质量逐渐减小
B. 氢离子在铜表面得e-
C. 电子从锌片经导线流向铜片
D. 电流从锌片经导线流向铜片
科目:高中化学 来源: 题型:
【题目】(1)现有下列A、B两组物质:
A组:CH3—CHCl—CH3、![]() 、HCOOH、CH3COOC2H5 。
、HCOOH、CH3COOC2H5 。
B组:CH3CH2CH2OH、银氨溶液、KOH溶液、Na2CO3溶液。 试回答:
①A组中_____________能跟B组中所有物质都可发生反应。
②B组中______________可跟A组中三种物质反应。
(2)苯的熔点为5.5℃,沸点为80.1℃,在寒冷的冬天怎样从细口的试剂瓶中取出苯___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把0.6molX气体和0.4molY气体混合于容积为2L的容器中,使其发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
nZ(g)+2W(g)。5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/( L· min),则n的值为
A. 1B. 2C. 3D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1。B为________极,A的电极反应为________________________。最终可观察到的现象是___________________________________________。
涉及的化学反应方程式有_______________________________。
(2)打开K1,合并K2。E为________极,F极的电极反应为_____,检验F极产生气体的方法是____________________________。
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是________,原因是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是
A. 配制溶液 B. 制取收集干燥氨气
B. 制取收集干燥氨气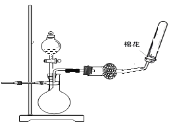
C. 除去粗盐中的不溶物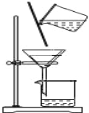 D. 观察Fe(OH)2的生成
D. 观察Fe(OH)2的生成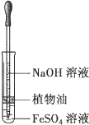
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某酸性溶液中含有Ba2+、Fe3+,则下述离子组中能与上述离子共存的是
A.NO3-、Cl-B.CO32-、Cl-C.NO3-、SO42-D.OH-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应 3A(g)+2B(g)![]() zC(g)+2D(g)。在2L的密闭容器中把4molA和2molB混合,2min后反应达到平衡时生成1.6 mol C,又测得D的反应速率v(D)= 0.2 mol.L-1min-1。则下列说法不正确的是( )
zC(g)+2D(g)。在2L的密闭容器中把4molA和2molB混合,2min后反应达到平衡时生成1.6 mol C,又测得D的反应速率v(D)= 0.2 mol.L-1min-1。则下列说法不正确的是( )
A. z=4B. B的转化率是40%
C. A的平衡浓度是1.4mol.L-1D. 平衡时气体压强是原来的![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com