
【题目】如下图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。

(1)打开K2,合并K1。B为________极,A的电极反应为________________________。最终可观察到的现象是___________________________________________。
涉及的化学反应方程式有_______________________________。
(2)打开K1,合并K2。E为________极,F极的电极反应为_____,检验F极产生气体的方法是____________________________。
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是________,原因是___________________________________________。
【答案】负O2+2H2O+4e-===4OH-溶液中有红褐色沉淀生成2Fe+O2+2H2O===2Fe(OH)2、4Fe(OH)2+O2+2H2O===4Fe(OH)3阴2Cl--2e-===Cl2↑用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气AE因为A极产生OH-,E极中H+反应了,促进了水的电离,溶液中有OH-剩余,酚酞遇OH-变红,所以溶液变红
【解析】
(1)打开K2,合并K1,装置为原电池,B为负极,A为正极,所发生的反应本质上是钢铁的吸氧腐蚀,故答案为:负、O2+2H2O+4e-==4OH-、溶液中有红褐色沉淀生成、2Fe+O2+2H2O===2Fe(OH)2、4Fe(OH)2+O2+2H2O===4Fe(OH)3;(2)打开K1,合并K2,装置为电解池,由于铁作阴极,所以该装置就是电解食盐水,故答案为:阴、2Cl--2e-===Cl2↑、用湿润的淀粉碘化钾试纸靠近F极,试纸变蓝,证明是氯气、AE、因为A极产生OH-,E极中H+反应了,促进了水的电离,溶液中有OH-剩余,酚酞遇OH-变红,所以溶液变红。


科目:高中化学 来源: 题型:
【题目】实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
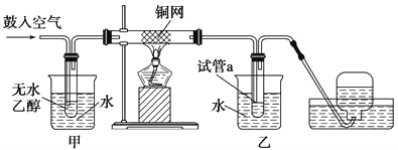
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式__________________ 、_____________________。
(2)在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是____________ 反应。进一步研究表明,鼓入空气的速率与反应体系的温度关系曲线如图所示。
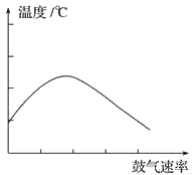
试解释出现图中现象的原因_______________________。
(3)甲和乙两个水浴作用不相同。甲的作用是_______________;乙的作用是______________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有_______。要除去该物质,可在混合液中加入________ (填写字母)。然后,再通过________________(填实验操作名称)即可除去。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期第ⅡA、ⅢA族金属元素的原子失去电子后,生成的阳离子的电子层结构( )。
A.与它同周期稀有气体元素原子的电子层结构相同
B.与它上一周期稀有气体元素原子的电子层结构相同
C.与它下一周期稀有气体元素原子的电子层结构相同
D.以上说法都不全面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 根据反应Cu+H2SO4![]() CuSO4+H2↑可推出Cu的还原性比H2的强
CuSO4+H2↑可推出Cu的还原性比H2的强
B. 电解含Pb(NO3)2和Cu(NO3)2的溶液,阴极上阳离子得电子次序依次是Cu2+、H+、Pb2+
C. 含amolNa2S的溶液最多能吸收2.5amol的二氧化硫气体(不考虑SO2在水中的溶解)
D. 由置换反应I2+2NaClO3===2NaIO3+Cl2可知I2的氧化性强于Cl2的氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示装置的叙述错误的是
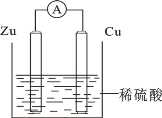
A. 锌是负极,其质量逐渐减小
B. 氢离子在铜表面得e-
C. 电子从锌片经导线流向铜片
D. 电流从锌片经导线流向铜片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+===SO2↑+H2O
B. 向氨水中加入少量H2C2O4溶液:H2C2O4 +2NH3·H2O ![]() C2O4 2—+2NH
C2O4 2—+2NH![]() +2H2O
+2H2O
C. 氢氧化钠溶液中加入铝粉:2Al+2OH- +6H2O === 2Al(OH)4-+3H2↑
D. 向CuSO4溶液中加入Na2O2:2Na2O2+2H2O===4Na++4OH-+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①CO(g)+![]() O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
下列说法正确的是( )
A. 通常状况下,氢气的燃烧热为241.8 kJ·mol-1
B. 由①可知,1 mol CO(g)和![]() mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量
mol O2(g)反应生成 1 mol CO2(g),放出283.0 kJ的热量
C. 可用下图表示2CO2(g)===2CO(g)+O2(g)反应过程中的能量变化关系
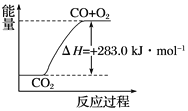
D. 分解1 mol H2O(g),其反应热为-241.8 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com