
X、Y、Z三种短周期元素,它们的原子序数之和为16 。X、Y、Z三种元素常见单质在常温下都是无色气体,在适当条件下可发生如下图所示变化:
已知一个B分子中含有的Z元素的原子个数比C分子中的少一个。请回答下列问题:
(1)X元素在周期表中的位置________ _。
(2)X的单质与Z的单质可制成新型的化学电(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入__________(填物质名称);负极电极反应式为___________________ _。
(3)C在一定条件下反应生成A的化学方程式是_______________________________。
(4)已知Y的单质与Z的单质生成C的反应是可逆反应,属于放热反应。将等物质的量的Y、Z的单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应。下列说法中,正确的是____________________(填写下列各项的序号)。
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y的单质的体积分数始终为50%
c.达到化学平衡时,Y、Z的两种单质在混合气体中的物质的量之比为11
d.达到化学平衡的过程中,混合气体平均相对分子质量减小
e.达到化学平衡后,再升高温度,C的体积分数增大
科目:高中化学 来源: 题型:
将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,此装置称为甲烷燃料电池。下列叙述中正确的是
①通入CH4的电极为正极; ②正极的电极反应式为:O2+2H2O+4e-=4OH-;
③通入CH4的电极反应式为:CH4+2O2+4e-=CO2+2H2O;
④负极的电极反应式为:CH4+10OH--8e-=CO32-+7H2O;
⑤放电时溶液中的阳离子向负极移动; ⑥放电时溶液中的阴离子向负极移动。
A.①③⑤ B.②④⑥ C.④⑤⑥ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
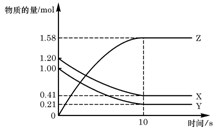 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是 ( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是 ( )
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B.反应开始到10s, X的物质的量浓度减少了0.79mol/L
C.反应开始时10s, Y的转化率为79.0%
D.反应的化学方程式为:X(g)+ Y(g) Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )
A.元素金属性:B>A;元素非金属性:D>C B.原子半径:A>B>C>D
C.离子半径:D(n+1)->Cn->B(n+1)+>An+ D.原子序数:b>a>c>d
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是 ( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
查看答案和解析>>
科目:高中化学 来源: 题型:
某浓度的氨水中存在下列平衡:NH3·H2O NH
NH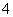 +OH-,若想增大NH
+OH-,若想增大NH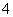 的浓度,而不增大OH-的浓度,应采取的措施是
的浓度,而不增大OH-的浓度,应采取的措施是
A.适当升高温度 B.加入NaOH固体
C.通入NH3 D.加入NH4Cl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:
A(g) + 2B(g) xC(g) ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
xC(g) ΔH=-192kJ·mol-1,向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
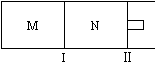
A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N)
B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N)
C.若x<3,C的平衡浓度关系为:c(M)>c(N)
D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101 kPa下,稀的强酸与强碱溶液反应的中和热为57.3 kJ/mol。
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程: 。
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。
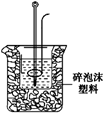 ①实验时所需的玻璃仪器除烧杯、量筒外还需: 。
①实验时所需的玻璃仪器除烧杯、量筒外还需: 。
②该装置中有一处错误是: ,如果用该错误
装置测定,结果会 (填“偏高”“偏低”“无影响”)
③如果该生用50 mL 0.25 mol/L的稀硫酸与50 mL 0.55 mol/L的稀烧
碱溶液,他用试剂的用量的理由是: 。在该实验中需要测
定某种数据,完成一次实验,需要测定该数据的次数为 次。使用正确的装置进
行实验,取上述溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中
和后生成的溶液的比热容为4.18J/(g·℃),溶液的密度均为1g/cm3。通过计算可得
中和热△H=
查看答案和解析>>
科目:高中化学 来源: 题型:
向四支试管中分别加入少量不同的溶液进行如下操作,结论正确的是
| 操作 | 现象 | 结论 | |
| A | 滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
| B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| C | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4 | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com