
【题目】常温下,HA的电离常数Ka=1×10-6,向20 mL浓度为0.01 mol·L-1的HA溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液的pH与加入NaOH溶液的体积之间的关系如图所示,下列说法正确的是( )
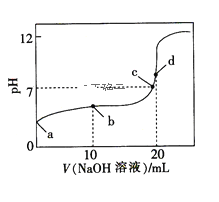
A.a点对应溶液的pH约为4,且溶液中只存在HA的电离平衡
B.b点对应溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-)
C.d点对应溶液中:c(OH-)-c(H+)=c(A-)
D.a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d
【答案】D
【解析】
A.a点为0.01 mol·L-1的HA溶液,此时溶液中存在HA和H2O的电离平衡,故A错误;
B.b点为在20mL0.01 mol·L-1的HA溶液中滴加10mL0.01 mol·L-1的NaOH溶液,此时溶液中NaH和HA等物质的量混合,溶液pH<7,说明HA的电离程度大于A-的水解程度,则c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-),故B错误;
C.d点为滴加20mLNaOH溶液,此时恰好完全中和生成NaA,溶液中存在的电荷守恒式为c(OH-)+c(A-)=c(H+)+c(Na+),物料守恒式为c(Na+)=c(A-)+c(HA),则c(OH-)-c(H+)=c(HA)<c(A-),故C错误;
D.a点为HA溶液,b点是HA和NaA等浓度的混合溶液,c点是NaA和少量HA的混合液且溶液pH=7,d点是NaA的溶液,酸、碱溶液都抑制了水的电离,NaA促进水的电离,且所含NaA的浓度越大,溶液中水的电离程度越大,则a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d,故D正确;
故答案为D。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)

根据以上信息填空:
(1)写出下列物质的化学式:A______ G__________ ;
(2)纯净的气体甲在气体乙中燃烧的现象:______________________________________;
(3)写出下列反应的离子方程式:反应①_________________________;反应④____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,如合成的金刚烷胺就是一种抗病毒药剂,对帕金森症、老年痴呆有良好的疗效.由环戊二烯合成金刚烷的路线如下:
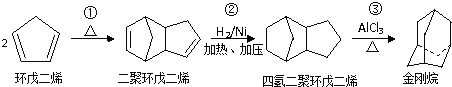
请回答下列问题:
(1)金刚烷的分子式为 ______ .
(2)反应①的反应类型是 ______ .
(3)金刚烷与四氢二聚环戊二烯的关系是 ______ .(填字母)
a 互为同系物 b 互为同分异构体 c 均为烷烃 d 均为环烃
(4)下面是以环戊烷为原料制备环戊二烯的合成路线:
![]()
其中,反应②的反应试剂和反应条件是 ______ ;X的名称是 ______ ;反应④的化学方程式是 ______ ;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(-CH3、-CH2R、-CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],则A的结构有 ______ 种(不考虑立体异构),其中核磁共振氢普为5组峰,且面积比为4:1:2:2:3的结构简式是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据SO2通入不同溶液中的实验现象,所得结论不正确的是( )
溶液 | 现象 | 结论 | |
A | 含HCl,BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2是酸性氧化物 |
B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有还原性 |
D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼和钒在炼钢、有机化工、高科技等领域有广泛应用。一种从炼油工业的废催化剂(主要成分为V2O5、MoO3、Al2O3、硫化物和碳氢化合物)中回收钼、钒的工艺流程如图:
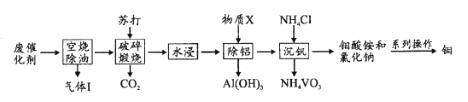
(1)“气体”除CO2、H2O外,还含有的主要成分是____。
(2)“破碎”的目的是____;缎烧中V2O5转化的化学方程式是____。
(3)加人物质X的目的是调节溶液pH除铝,X的化学式是____。
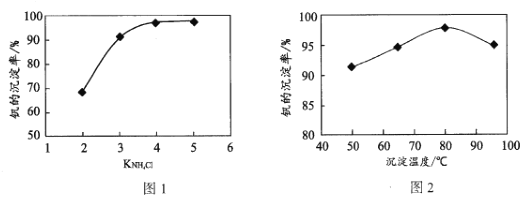
(4)“沉钒”过程中控制pH为8.35,其他条件一定时,钒的沉淀率与加铵系数KNH4Cl、温度的关系分别如图1、图2,则应选择的加铵系数是____;温度超过80°C时,钒的沉淀率下降的原因是____。
(5)钼酸铵[(NH4)2MoO4]在高温下通入H2可制得单质钼,该过程的化学方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环中不存在碳碳单键和碳碳双键交替的结构,可以作为证据的事实是( )
①苯是无色易挥发的液体;
②苯不能使酸性高锰酸钾溶液褪色;
③![]() 和
和 是同一种物质。
是同一种物质。
A. ①②③ B. ①和② C. ①和③ D. ②和③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】喹啉是合成药物的中间体,一种合成喹啉的路线如图:

(1)A→B所需的试剂为_____。
(2)两分子B在一定条件下生成C和乙醇,化合物B断键的位置为_____(填序号)
(3)C→D的反应类型为_____,D→E的反应方程式是_____。
(4)化合物G中,除亚氨基外还含有的官能团名称是_____。
(5)F的同分异构体W能与碳酸氢钠溶液反应放出气体,且能使溴水褪色,其中核磁共振氢谱峰面积比为6:1:1。W的结构简式为_____。
(6)参照上述路线,设计以苯胺(![]() )和
)和 制备的
制备的 合成路线(无机试剂任选)_____。
合成路线(无机试剂任选)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.向硫酸铜溶液中加入铁片:3Cu2++2Fe=2Fe3++3Cu
B.石灰石与醋酸反应:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
C.碳酸氢铵与足量热的NaOH溶液反应:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D.向Ba(OH)2溶液中加入少量NaHSO3溶液:2HSO3-+Ba2++2OH-= BaSO3↓+SO32-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com