
【题目】将250mL密度1.31g/cm3、质量分数为15%的硫酸与适量的铁屑充分反应.计算:
(1)此硫酸溶液中H2SO4的物质的量浓度;
(2)生成的H2的体积(标况);
(3)将生成的FeSO4配成400mL溶液,此溶液中Fe2+的物质的量浓度.
【答案】
(1)解:密度1.31g/cm3、质量分数为15%的硫酸,
由c= ![]() 可知,c=
可知,c= ![]() =2.0mol/L,
=2.0mol/L,
答:此硫酸溶液中H2SO4的物质的量浓度为2mol/L
(2)解:H2SO4的物质的量为0.25L×2.0mol/L=0.5mol,
由H2SO4~H2可知,H2的物质的量为0.5mol,
则H2的体积为0.5mol×22.4L/mol=11.2L,
答:生成的H2的体积为11.2L
(3)解:H2SO4的物质的量为0.25L×2.0mol/L=0.5mol,
由H2SO4~FeSO4可知,FeSO4的物质的量为0.5mol,
则Fe2+的物质的量浓度为 ![]() =1.25mol/L,
=1.25mol/L,
答:溶液中Fe2+的物质的量浓度为1.25mol/L
【解析】(1)根据c= ![]() 来计算;(2)根据H2SO4~H2来分析H2的物质的量,然后利用V=n×Vm来计算其体积;(3)根据H2SO4~FeSO4来分析FeSO4的物质的量,再利用c=
来计算;(2)根据H2SO4~H2来分析H2的物质的量,然后利用V=n×Vm来计算其体积;(3)根据H2SO4~FeSO4来分析FeSO4的物质的量,再利用c= ![]() 来计算.
来计算.


科目:高中化学 来源: 题型:
【题目】鉴别CH3OCH3和CH3CH2OH可采用化学方法和物理方法,下列方法不能对二者进行鉴别的是( )
A.利用金属钠或金属钾
B.利用质谱法
C.利用红外光谱
D.利用核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯化镁和氯化铝的200 mL 混合溶液中,c(Mg2+)为 0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为( )
A. 40 mL B. 72 mL C. 80 mL D. 128 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲除去下列物质中混有的少量杂质(括号内物质为杂质),错误的是( )
A.苯(苯酚):氢氧化钠溶液,充分震荡静止后,分液
B.乙醇(水):加入新制生石灰,蒸馏
C.溴苯(溴):加入氢氧化钠溶液,充分震荡静止后,分液
D.乙酸(乙醇):加入金属钠,蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的X和Y两种原子,化学性质一定相似的是( )
A.X原子和Y原子最外层都只有1个电子
B.X原子的核外电子排布式为1s2 , Y原子的核外电子排布式为1s22s2
C.X原子的2p能级上有3个电子,Y原子的3p能级上有3个电子
D.X原子核外M层上仅有2个电子,Y原子核外N层上仅有2个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色发展”是党的十九大进一步强调的治国理念。下列做法不符合这一理念的是( )
A.随意丢弃废旧电池B.提倡使用生态肥料C.推广清洁能源汽车D.合理开采稀土资源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图图示与对应的叙述相符的是( ) 
A.图甲表示反应:4CO(g)+2NO2(g)N2(g)+4CO2(g)△H<0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2 , K1>K2
B.图乙表示压强对可逆反应2A(g)+2B(g)3C(g)+D(g)的影响,乙的压强比甲的压强大
C.图丙表示的反应是吸热反应,该图表明催化剂能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥的有色布条和湿润的有色布条的广口瓶,可观察到的现象是__________________________________.
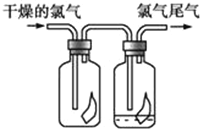
(2)写出C12与水反应的化学方程式________________________
(3)为防止氯气污染空气,可用氢氧化钠溶液吸收多余的氯气,原理是________________(用化学方程式表示).根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________(填化学式,下同)。
(4)氯气泄漏时,人们需尽快远离现场,可用浸有一定浓度某物质水溶液的毛巾捂住口鼻,最适宜采用的物质是__________.
A.NaOH B.NaCl C.KBr D.Na2CO3.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com