
【题目】将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:NH4Br(s) ![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g) ![]() Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用
Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用![]() (NH3)表示,下列反应速率正确的是
(NH3)表示,下列反应速率正确的是
A.0.5mol/(L·min) B.2.5 mol/(L·min)
C.2 mol/(L·min) D.5 mol/(L·min)
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中。“硫酸法”生产钛的原料是钛铁矿[主要成分是钛酸亚铁(FeTiO3),含有Fe(Ⅲ)等杂质],同时获得副产品甲的工业生产流程如下:
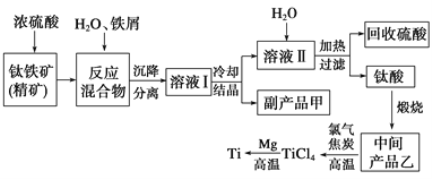
(1)浓硫酸处理钛铁矿时产物之一是TiOSO4,反应中无气体放出,写出该反应的化学方程式___。
(2)上述生产流程中加入铁屑的目的是_______________,可循环利用的物质是_________,检验副产品甲是否变质的实验方法是_________________________________。
(3)溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当pH等于_________时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该沉淀是_______________________________________。
(4)中间产品乙是一种氧化物,其经高温与氯气、焦炭反应,除生成TiCl4外,还生成了一种可燃性气体,请写出该反应的化学方程式___________。
(5)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还原控制的反应条件是__________________________________,反应后的产物需要加入______________溶解后才能达到提纯金属钛的目的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] 俗称莫尔盐,可溶于水,在100℃~110℃时分解。在定量分析中常用作标定重铬酸钾、高锰酸钾等溶液的标准物质,还用于冶金、电镀等。
Ⅰ.化学课外活动小组研究莫尔盐晶体强热时的分解产物。
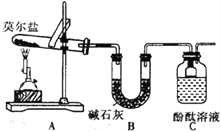
(1)甲组同学按照如图所示的装置进行研究,装置C中可观察到的现象是__________,由此可知分解产物中有____________。
(2)乙组同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2。为进行验证,选用甲组实验中的装置A和下图所示的部分装置进行实验。
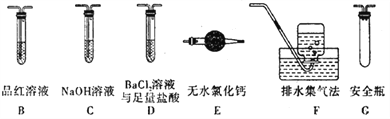
①乙组同学的实验中,装置依次连接的合理顺序为A、____________。
②含有SO3的实验现象是______________;
Ⅱ.为测硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500mL溶液。甲、乙、丙三位同学设计了如下三个实验方案,请回答:
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol·L-1的酸性KMnO4溶液分三次进行滴定。
乙方案:取25.00 mL硫酸亚铁铵溶液进行如下实验。
![]()
丙方案:(通过![]() 测定)实验设计图如下所示。取25.00mL硫酸亚铁铵溶液进行该实验。
测定)实验设计图如下所示。取25.00mL硫酸亚铁铵溶液进行该实验。
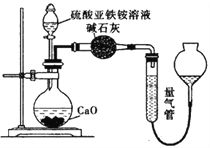
(1)甲方案中的离子方程式为___________,若实验操作都正确,但其测定结果总是小于乙方案,可能原因为___________。
(2)乙方案中沉淀是否洗涤干净的检验方法是________________。
(3)丙方案中量气管中最佳试剂是______________。
a.水 b.饱和NaHCO3溶液 c.CCl4
(4)若测得NH3(已折算为标准状况下)为V L,则硫酸亚铁铵纯度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各金属及其化合物的说法正确的是( )
A. 已知 CCl4 不可燃,故少量的 Na 可保存在 CCl4 液体中
B. 金属铝既可与酸反应也可与碱反应,故铝是两性金属
C. 明矾为金属铝的化合物,可用作净水剂
D. 生铁和钢都属于铁合金,两者抗腐蚀性都很强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E代表单质或化合物,它们之间的相互转换关系如图所示.A为地壳中含量仅次于氧的非金属元素的单质. 
请填空:
(1)形成单质A的原子的结构示意图为 , 它的最高化合价为 .
(2)B的化学式(分子式)为 , B和碳反应生成A和E的化学方程式是 .
(3)C的化学式(分子式)为 , D的化学式(分子式)为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产和生活密切相关,下列说法正确的是( )
A.铁制品表面镀锡不能增强铁制品的抗腐蚀性
B.被Cu2+污染的水体可以用难溶的FeS进行治理
C.施用化肥时,将草木灰与氯化铵混合使用可增加肥效
D.世界能源大会将核能作为碳能源重要替代品,核电站能够把化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.![]() =1×10﹣13mol?L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
=1×10﹣13mol?L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D.水电离的c(H+)=1×10﹣13mol?L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com