
����Ŀ��[��ѧһѡ��5���л���ѧ����]��15�֣�����������������PPG����һ�ֿɽ���ľ�����߷��Ӳ��ϣ��ڲĖ������������Է����кܺõ�Ӧ��ǰ���� PPG��һ�ֺϳ�·�����£�

��֪��
����A����Է�������Ϊ70���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⣻
��������BΪ���ȴ�����������C�ķ���ʽΪC5H8��
��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ�
��![]() ��
��
�ش��������⣺
��1��A�Ľṹ��ʽΪ ��
��2����B����C�Ļ�ѧ����ʽΪ ��
��3����E��F����G�ķ�Ӧ����Ϊ ��G�Ļ�ѧ����Ϊ ��
��4������D��H����PPG�Ļ�ѧ����ʽΪ ��
����PPGƽ����Է�������Ϊ10000������ƽ���ۺ϶�ԼΪ �����ţ���
a��48 b��58 c��76 d��122
��5��D��ͬ���칹������ͬʱ�������������Ĺ��� �֣����������칹����
�����뱥��NaHCO3��Һ��Ӧ��������
�����ܷ���������Ӧ�����ܷ���������Ӧ
���к˴Ź���������ʾΪ3��壬�ҷ������Ϊ6��1��1���� ��д�ṹ��ʽ����
D������ͬ���칹�����������ֱ�����������ʾ���źţ������ݣ���ȫ��ͬ����������_____�����ţ���
a�������� b����������� c��Ԫ�ط����� d���˴Ź�����
���𰸡���1��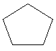 ��2��
��2��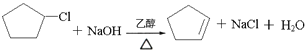
��3���ӳɷ�Ӧ��3���ǻ���ȩ�����¡��ǻ���ȩ����4����
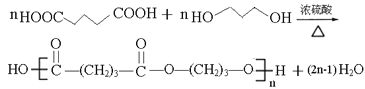
��b��5��5��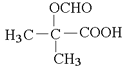 ��c
��c
��������
��A����Է�������Ϊ70���˴Ź���������ʾֻ��һ�ֻ�ѧ�������⣬![]() =5��10����AΪC5H10���ṹΪ
=5��10����AΪC5H10���ṹΪ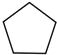 ��A����������ȡ����Ӧ����BΪ
��A����������ȡ����Ӧ����BΪ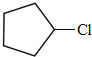 ��B������ȥ��Ӧ����CΪ
��B������ȥ��Ӧ����CΪ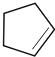 ��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC(CH2)3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪHOCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪHOCH2CH2CH2OH��D��H�������۷�Ӧ����PPG(
��������C�ķ���ʽΪC5H8��C����������Ӧ����DΪHOOC(CH2)3COOH��E��FΪ��Է���������14��ͬϵ�F�Ǹ������ֵ����ʣ���FΪHCHO����֪EΪCH3CHO������Ϣ�ܿ�֪E��F��Ӧ����GΪHOCH2CH2CHO��G�����������ӳɷ�Ӧ����HΪHOCH2CH2CH2OH��D��H�������۷�Ӧ����PPG(![]() )��
)��
(1)A�Ľṹ��ʽΪ ��
��
(2)��B����C�Ļ�ѧ����ʽΪ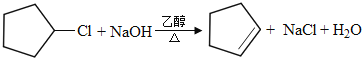 ��
��
(3)��E��F����G�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��G�Ļ�ѧ����Ϊ3-�ǻ���ȩ��
(4)����D��H����PPG�Ļ�ѧ����ʽΪ![]() ��
��
����PPGƽ����Է�������Ϊ10000������ƽ���ۺ϶�ԼΪ![]() ��58���ʴ�Ϊb��
��58���ʴ�Ϊb��
(5)D��ͬ���칹������ͬʱ��������뱥��NaHCO3��Һ��Ӧ�������壬��-COOH���ڼ��ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ-COOCH��D�й�5��C����3��C-C-C�ϵ�2��H��-COOH��-OOCHȡ������Ϊ3+2=5�֣������к˴Ź���������ʾΪ3��壬�ҷ������Ϊ6��1��1����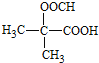 ��
��
(6)D��ͬ���칹����Ԫ�������ͬ��������Ԫ�ط�������ʾ���ź�(������)��ȫ��ͬ����ѡc��


 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���밴Ҫ��ش��������⣺
��1�����Ĺ����ŵ�������_____��
��2��ij��̬�л���������������ܶ�Ϊ14������ṹ��ʽΪ_____��
��3��ij�л���Ľṹ��ʽ��ͼ��ʾ������һ�ȴ��ﹲ��_____�֡�

��4����������ϵͳ����������ӦΪ_____��
��5���ֱ����ʵ�����C3H8��C4H8��ȫȼ�գ������������������_____�������ʽ����
��6���������ʽ�У�ֻ�ܴ���һ���л������_____��ѡ���Ӧ����ţ���
��CH3 ��CH2 ��CH2O ��CH4O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I���������¼������ʢ����ᡢ�ڴ��ᡢ���������ơ����Ȼ�李��ݴ����ơ������������ơ��߰�ˮ����ش���������:
��1��������������������ʵ���______________������ţ���
��2�������¢ܵ���ҺpH_____7���>����<����=������ԭ��__________�������ӷ���ʽ��ʾ����
��3����ˮ��Һ�г����ԣ�ԭ����__________________________��
��4��������,��aL pH=11��NaOH��Һ��bL pH=1��HNO3��Һ���(���Ի�Ϻ���Һ����ı仯),�����û����Һ��pH=2����a:b=________��
��5����֪��a�������£������NH3H2O�ĵ���ƽ�ⳣ����Ϊ1.74��10-5��
b��CH3COOH+NaHCO3�TCH3COONa+CO2��+H2O
��CH3COONH4��Һ��______�ԣ���ᡱ��������С�����ͬ����NH4HCO3��Һ��______�ԡ�
��6�����ڴ�����Һ�ʹ�������Һ������˵����ȷ����____________��
A��ϡ�ʹ�����Һ������ĵ���̶�����ϡ�ʹ�������Һ������Ƶ�ˮ��̶ȼ�С��
B�������¶ȿ��Դٽ�������룬Ҳ���Դٽ�������ˮ�⡣
C������ʹ����ƻ��Һ�У��������ƴ����Ƶ�ˮ�⡢������Ҳ���ƴ���ĵ��롣
D�������£�����ʹ����Ƶ������Ũ�Ȼ�ϣ���Һ�ʼ��ԡ�
II��25��ʱ����ʢ��50mL pH=3��HA��Һ�ľ��������м���pH=13��NaOH��Һ������NaOH��Һ�����(V)�����û����Һ���¶�(T)�Ĺ�ϵ��ͼ��ʾ��
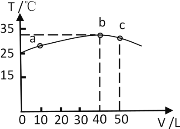
��7����ͼ�����Ƴ�HA��Һ�����ʵ���Ũ��Ϊ_______________��25��ʱ��pH=3��HA��Һ�ĵ����Ϊ______________��
��8��b����Һ������Ũ���ɴ�С��˳��Ϊ_______________________��
��9������NaOH��Һ����Һ������ʱ������ͼ�е�λ��_________���b��ǰ�� ��b�㡱��b�������Һ������ʱ�����ڣ�c(A��)______c(Na��)���>����<����=������
III����10����֪��Ksp[Al(OH)3]��1��10��33�� pH��7.1ʱMn(OH)2��ʼ�����������£���ȥMnSO4��Һ�е�Al3��(ʹ��Ũ��С��1��10��6 mol��L��1)���������ҺpH��ΧΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D���ֶ�����Ԫ�أ�ԭ������D��A��B��C����A��Bͬ���ڣ�C��Dͬ���壬A��ԭ�ӽṹʾ��ͼ��ͼ��BԪ�������������Ǵ������������ķ�֮һ��CԪ�ص���̬�⻯���ˮ��Һ�Լ��ԣ��ݴ���գ�

��1��AԪ����̬�⻯��ĵ���ʽ___��A��B��C��D����Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳������Ϊ___������Ԫ�ط��ţ�
��2��A��������������������Ʒ�Ӧ�����ӷ���ʽΪ___��
��3��A��C��D������������Ӧˮ���������ǿ��_______��C���⻯���D���⻯��е�___����������������������ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼȲ���ʹ��ˮ��ɫ���ֲ���ʹ���Ը��������Һ��ɫ����
������ ����ϩ ����Ȳ �ܱ� �ݼױ� �������� �߾۱�ϩ ���ϩ
A. �٢ڢۢ� B. �٢ܢ� C. �٢ܢޢ� D. �ڢۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A. ���廯������Һ��ͨ������������2Fe2����Cl2===2Fe3����2Cl��
B. ��������Һ��ͨ������CO2��2C6H5O����CO2��H2O�D��2C6H5OH��CO![]()
C. ������������Һ�е�������������Һ�����ԣ�H����SO![]() ��Ba2����OH��===BaSO4����H2O
��Ba2����OH��===BaSO4����H2O
D. ������������ĩ����������У�Fe(OH)3��3H��===Fe3����3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Ϊ��Ԫ��������£���ijŨ�ȵIJ�����Һ����μ���һ����Ũ�ȵ�KOH��Һ��������Һ��H2C2O4��HC2O4����C2O42�������������ʵ����������ģ�����ҺpH�Ĺ�ϵ��ͼ��ʾ��������˵���в���ȷ����
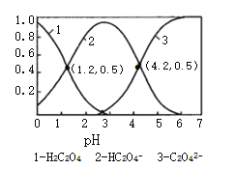
A. pH=1.2��Һ�У�c��K+��+c��H+���Tc��OH����+c��H2C2O4��
B. H2C2O4�ĵ�һ�����룬ƽ�ⳣ��Ϊ10-1.2
C. ����ͬ���ʵ���KHC2O4��K2C2O4������ȫ����ˮ���û��Һ��pHΪ4.2
D. ��pH=1.2����Һ�м�KOH��Һ��pH������4.2�Ĺ�����ˮ�ĵ���̶�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�����£���0.1mol��L��1��HCl��Һ��ˮϡ��10����������Һ��pH=2
B.�����£�pH=3��HCl��Һ��pH=11��NaOH��Һ�У�c(Cl)=c(Na+)
C.0.1mol��L��1��NaOH��Һ������CH3COOH��Һ��ϣ���������Һ�����ԣ���c(CH3COOH)��0.1mol��L��1
D.��������ˮʱ��ˮ�����ӻ�����Kw����c(H+)������c(OH)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪͭпԭ��ص�ʾ��ͼ������˵���������
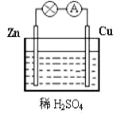
A. һ��ʱ���пƬ���ܽ⣬������С
B. ��װ���ܽ�����ת��Ϊ��ѧ��
C. ��ͭƬ����ʯī�����������Ȳ���
D. ͭ������������ԭ��Ӧ��ֻ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com