
【题目】室温下向10mL 0.1 molL﹣1NaOH溶液中加入0.1molL﹣1的一元酸HA溶液pH的变化曲线如图所示.下列说法正确的是( ) 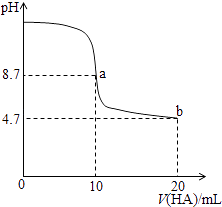
A.a点所示溶液中c(Na+)>c(A﹣)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A﹣)+c(HA)
D.b点所示溶液中c(A﹣)>c(HA)
【答案】D
【解析】 解:A.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性,应为c(HA)>c(H+),故A错误;
B.a点A﹣水解,促进水的电离,b点时HA过量,溶液呈酸性,HA电离出H+ , 抑制水的电离,故B错误;
C.pH=7时,c(H+)=c(OH﹣),由电荷守恒可知c(Na+)+c(H+)=c(A﹣)+c(OH﹣),则c(Na+)=c(A﹣),故C错误;
D.b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA电离程度大于A﹣水解程度,则存在c(A﹣)>c(HA),故D正确.
故选D.
A.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性;
B.b点时HA过量,溶液呈酸性,HA电离出H+ , 抑制水的电离; C.pH=7时,c(H+)=c(OH﹣),结合电荷守恒判断;D.b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA电离程度大于A﹣水解程度.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】教材中用酸性KMnO4溶液和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图一和表: 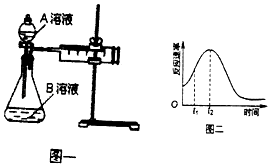
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 molL﹣1H2C2O4溶液 | 30 mL 0.01 molL﹣1kMnO4溶液 |
② | 20 mL 0.2 molL﹣1 | 30 mL 0.01 molL﹣1KMnO4溶液 |
(1)用电离方程式表示草酸溶液显酸性的原因
(2)该实验探究的是因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是①②(填“>”“<”“=”)
(3)若实验①在2min末收集了896mL CO2(标准状况下),则用MnO4﹣表示该时间内的化学反应速率为v (MnO4﹣)= .
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定来比较化学反应速率.
(5)该实验小组同学发现反应速率如图二所示,其中t1~t2时间内速率变快的主要原因可能是:①该反应放热、② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积均为10 mL、物质的量浓度相同的两份NaOH 溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是

A. 原NaOH溶液的物质的量浓度为0.5 mol/L
B. 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3-
C. 乙溶液中含有的溶质是Na2CO3、NaOH
D. 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下N2+3H2=2NH3为放热反应,下列说法正确的是( )
A.该反应是可逆反应
B.反应达到平衡时,反应速率为零
C.氢气可以完全转化为氨气
D.反应物的总能量小于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有100mL1mol·L-1稀硫酸的烧杯中,缓慢加入铁粉和铜粉的混合物,并用玻璃棒不断地搅拌,下图是溶液中的某种微粒(X) 的物质的量随加入混合物质量变化的关系图。下列说法一定正确的是( )
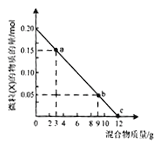
A. 该金属混合物中,铁粉的质量分数约为15.6%
B. a点时,再向烧杯中加入KNO3固体,无明显现象
C. b点时,再向烧杯中滴加0.1mol·L-1的NaOH溶液,立刻产生白色沉淀
D. C点时,再向烧杯中通入Cl20.16mol充分反应,铜粉完全溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里有4个药品橱,已经存放以下物品:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 盐酸,硫酸 | 氢氧化钠,氢氧化钙 | 红磷,硫 | 铜,锌 |
实验室新购进一些碘,应该将这些碘放在( )
A.甲橱B.乙橱C.丙橱D.丁橱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,某学习小组为了探究二氧化硫的某些性质,进行了如下实验。
I.如下图所示,使用药品和装置一探究二氧化硫的还原性:
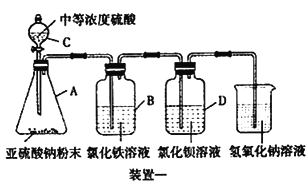
(1)装置C的名称为________。
(2)B中溶液的现象为________。
(3)学生甲预测装置D 中没有白色沉淀产生,但随着反应的进行,发现D 中产生了少量白色沉淀。学生乙经过查阅资料发现少量白色沉淀可能是硫酸钡,因为装置或溶液中少量的氧气参与了氧化反应,请写出装置D 中的反应方程式________。
II.经过思考,设计了如下装置二,且所配制的溶液均使用无氧蒸馏水,检验SO2 在无氧干扰时,是否与氯化钡反应生成沉淀。
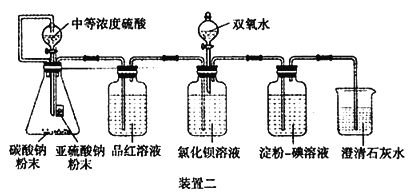
(4)碳酸钠粉末的目的是________。
(5)当______时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(6)裝置二选用澄清石灰水而不用氢氧化钠溶液的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3的性质说法正确的是
A. 溶解度:Na2CO3>NaHCO3
B. 右图所示装置可证明稳定性:Na2CO3>NaHCO3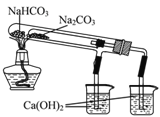
C. 用澄清石灰水可鉴别Na2CO3溶液和NaHCO3溶液
D. 等质量的Na2CO3和NaHCO3分别与过量盐酸反应,放CO2质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
B | 向无色溶液中加硝酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中一定含SO |
C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
D | 向某溶液中先加氯水再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定含Fe2+ |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com