
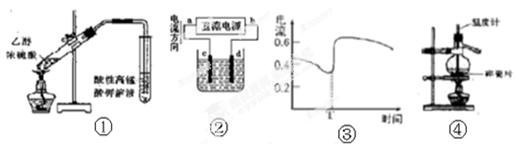
| A.装置①检验加热时产生的乙烯 |
| B.装置②精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液。 |
| C.图③表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 |
| D.装置④分离溴的四氯化碳溶液 |
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
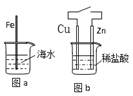
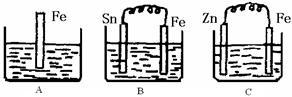
| A.图a,负极上发生的反应是:O2+4e+2H2O → 4OH- |
| B.图b,接通开关后溶液中的H+向正极移动 |
| C.图a,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D.图b,接通开关后Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
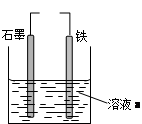
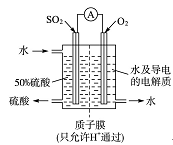
| A.若两电极直接连接,a是食盐水,则发生析氢腐蚀 |
| B.若两电极直接连接,则电子从铁流向石墨 |
| C.若铁接电源负极,石墨接电源正极,a是稀H2SO4溶液,电解一段时间后溶液的pH增大 |
| D.若铁接电源正极,石墨接电源负极,a是氯化铜溶液,阴离子向石墨电极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
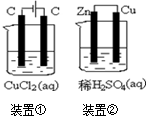
| A.两个装置中都发生了化学变化,都由化学能转变为电能 |
| B.装置②中电流方向是从Zn经导线流入Cu |
| C.反应开始阶段,两个装置中均有氢气产生 |
| D.电极反应式:阳极 2Cl—-2e-→Cl2↑正极 2H++2e-→H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
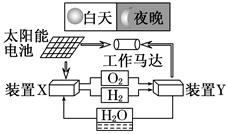
| A.该系统中只存在三种形式的能量转化 |
| B.装置Y中负极的电极反应式为:O2+2H2O+4e-===4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
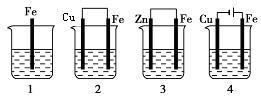
| A.1中的铁被腐蚀得最快 |
| B.2中的铁被腐蚀得最慢 |
| C.3中是电化学防腐蚀的运用,称为牺牲阳极的阴极保护法 |
| D.4中装置也能起到防止铁被腐蚀的作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com