

分析 某金属是日常生活中应用最广泛的金属,为Fe,废铜中含有不溶于酸的杂质及少量Fe,得到的副产物是Fe2O3,废铜酸浸,最后得到胆矾,根据元素守恒知,该酸是硫酸,得到的滤液I中含有硫酸铜、硫酸亚铁,向溶液中加入双氧水,双氧水能氧化亚铁离子生成铁离子,加入试剂a并调节溶液的pH,加入的试剂能使铁离子转化为沉淀且不能引进新的杂质,可以加入和酸反应的物质来调节溶液的pH并且不能产生新的杂质,然后煮沸除去溶液中溶解的气体,将得到的沉淀灼烧得到红棕色氧化物Fe2O3,将溶液蒸发浓缩、冷却结晶、过滤、干燥得到胆矾,结合题目分析解答.
解答 解:某金属是日常生活中应用最广泛的金属,为Fe,废铜中含有不溶于酸的杂质及少量Fe,得到的副产物是Fe2O3,废铜酸浸,最后得到胆矾,根据元素守恒知,该酸是硫酸,得到的滤液I中含有硫酸铜、硫酸亚铁,向溶液中加入双氧水,双氧水能氧化亚铁离子生成铁离子,加入试剂a并调节溶液的pH,加入的试剂能使铁离子转化为沉淀且不能引进新的杂质,可以加入和酸反应的物质来调节溶液的pH并且不能产生新的杂质,然后煮沸除去溶液中溶解的气体,将得到的沉淀灼烧得到红棕色氧化物Fe2O3,将溶液蒸发浓缩、冷却结晶、过滤、干燥得到胆矾,
(1)滤液I中亚铁离子和双氧水发生氧化还原反应生成铁离子和水,加入H2O2后反应的离子方程式2Fe2++2H++H2O2=2Fe3++2H2O,
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(2)加入和酸反应的物质来调节溶液的pH并且不能产生新的杂质,BDE都能和酸反应生成硫酸铜且不能引进新的杂质,AC引进新的杂质,故选BDE;
(3)煮沸的目的是除去溶解的二氧化碳,防止生成碳酸铜,故答案为:除去溶解的二氧化碳.
点评 本题考查物质分离和提纯,为高频考点,侧重考查学生分析判断能力,涉及基本操作、物质性质、物质分离提纯等知识点,明确流程图中发生的反应及基本操作方法、物质的性质是解本题关键,注意(2)中除杂剂的选取,题目难度不大.


科目:高中化学 来源: 题型:解答题
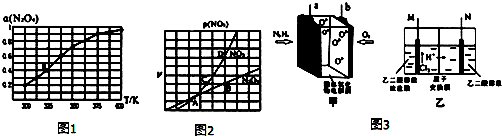
| 化学键 | N-H | N-N | N≡N | O-H |
| E/(kJ•mol-1) | 390 | 190 | 946 | 460 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
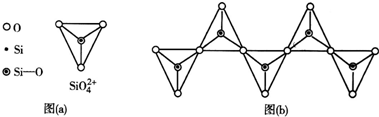
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
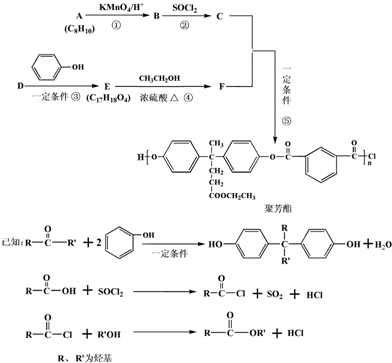
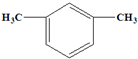 .
. .
.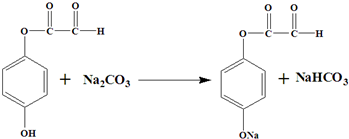 或
或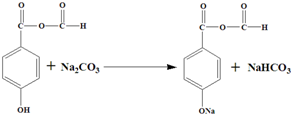 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀硫酸除钢铁表面的铁锈利用了硫酸的酸性 | |
| B. | 干冰用于人工降雨,是利用了干冰升华吸热 | |
| C. | 胃药中含氢氧化镁是因为氢氧化镁能给人提供镁元素 | |
| D. | 碳酸氢钠作焙制糕点的发酵粉是利用了碳酸氢钠能与发醇面团中的酸性物质反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8.0gCuO和Cu2S的混合物含铜原子个数为0.2NA | |
| B. | 标准状况下,11.2L乙醇蒸气含共价键数目为4NA | |
| C. | 1molK与O2完全反应生成K2O、K2O2、KO3的混合物,转移电子数为NA | |
| D. | 1L0.2mol•L-1NH4ClO4溶液中含NH4+数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫具有较强的还原性,故不能用浓硫酸干燥 | |
| B. | 苯、溴水、铁粉混合可制成溴苯 | |
| C. | 苯在一定条件下既能发生取代反应,又能发生加成反应,但不能发生氧化反应 | |
| D. | FeCl3溶液可以腐蚀线路板上的Cu,不能说明Cu的金属活动性大于Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
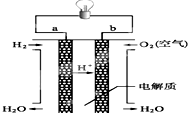 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com