
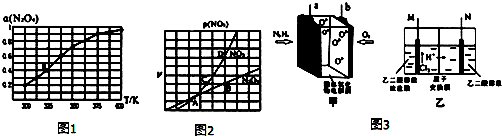
| ��ѧ�� | N-H | N-N | N��N | O-H |
| E/��kJ•mol-1�� | 390 | 190 | 946 | 460 |
���� ��1����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ�
��2���������¶�ƽ�������ȷ����ƶ�����С��ϵѹǿ���Ƴ�NO2��ʹƽ�������ƶ���
�ڻ�ѧƽ�ⳣ��K=$\frac{�������ѹ��֮��}{��Ӧ���ѹ��֮��}$��
�ۻ�ѧƽ�ⳣ��Kp=[p��NO2��]2��p��N2O4�������ߵķ�Ӧ����֮�ȵ����������֮�ȣ�����ƽ�������ԣ�NO2��=2�ԣ�N2O4����Ϊƽ��㣻
��3����ȼ��������������������Ӧ��
�ڸ���ͼ֪��a��Ϊ������M�缫�����������ɣ�˵��M�缫�������ӷŵ�������������MΪ������NΪ����������������������N�缫���Ҷ���õ��Ӻ������ӷ�Ӧ������ȩ�
������1.5molH+ͨ�����ӽ���Ĥ������ȫ�����˷�Ӧ������HOOC-COOH+2e-+2H+�THOOC-CHO+H2O֪�ұ�װ����0.75mol��ȩ�����ɣ�M�缫���������ķ�Ӧ����ʽΪCl2+OHC-CHO+H2O�THOOC-CHO+2HCl���ݴ˼����װ��������ȩ������ʵ�����
��� �⣺��1����1mol N2O4��1����ȫ�ֽ����Ӧ��ԭ��ʱ��Ҫ���յ�����QKJ����
190kJ/mol��2+390kJ/mol��8+QkJ/mol-946kJ/mol��3-460kJ/mol��8=-1225 kJ/mol��
���Q=1793���ʴ�Ϊ��1793kJ��
��2���ٸ���ͼ֪�������¶�ת�������������¶�ƽ�������ȷ����ƶ���������Ӧ�����ȷ�Ӧ����Ҫ���N2O4ת���ʣ����ı䷴Ӧ�¶��⣬������ʩ�м�С��ϵѹǿ���Ƴ�NO2��
�ʴ�Ϊ��������С��ϵѹǿ���Ƴ�NO2��
��������������ת������0.4����ԭ���������������ʵ���Ϊxmol��ת�������ʵ���Ϊ0.8xmol��������������ʵ���=��x-0.4x+0.8x��mol=1.4xmol����ͬ�����£������ѹǿ֮�ȵ��������ʵ���֮�ȣ����Է�Ӧ��ѹǿ=$\frac{108KPa}{xmol}$=151.2KPa��
�����������ķ�ѹ=151.2KPa��$\frac{0.6xmol}{1.4xmol}$=64.8KPa��
���������ķ�ѹ=151.2KPa��$\frac{0.8xmol}{1.4xmol}$=86.4KPa��
��ѧƽ�ⳣ��K=$\frac{�������ѹ��֮��}{��Ӧ���ѹ��֮��}$=$\frac{86��{4}^{2}}{64.8}$=115.2��
�ʴ�Ϊ��115.2��
�ۻ�ѧƽ�ⳣ��Kp=[p��NO2��]2��p��N2O4�������ߵķ�Ӧ����֮�ȵ����������֮�ȣ�
���Ԧԣ�NO2�����ԣ�N2O4��=k2[p��NO2��]2��k1•p��N2O4��=2��1��
��ѧƽ�ⳣ��Kp=[p��NO2��]2��p��N2O4����
��K1=$\frac{1}{2}$K2��Kp��
����ƽ�������ԣ�NO2��=2�ԣ�N2O4����Ϊƽ��㣬BD���ѹǿ֮�ȵ����䷴Ӧ����֮��Ϊ1��2������BDΪƽ��㣬
�ʴ�Ϊ��$\frac{1}{2}$K2��Kp��B����D�㣻
��3����ȼ��������������������Ӧ���缫��ӦʽΪN2H4+2O2-4e-=N2+2H2O���ʴ�Ϊ��N2H4+2O2-4e-=N2+2H2O��
�ڸ���ͼ֪��a��Ϊ������M�缫�����������ɣ�˵��M�缫�������ӷŵ�������������MΪ������NΪ����������������������N�缫���Ҷ���õ��Ӻ������ӷ�Ӧ������ȩ�ᣬ�缫��ӦʽΪHOOC-COOH+2e-+2H+�THOOC-CHO+H2O���ʴ�Ϊ��N��HOOC-COOH+2e-+2H+�THOOC-CHO+H2O��
������2molH+ͨ�����ӽ���Ĥ������ȫ�����˷�Ӧ������HOOC-COOH+2e-+2H+�THOOC-CHO+H2O֪�ұ�װ����1mol��ȩ�����ɣ�M�缫���������ķ�Ӧ����ʽΪCl2+OHC-CHO+H2O�THOOC-CHO+2HCl����1.5mol����������ʱͬʱ������ȩ��0.75mol����������1.5molH+ͨ�����ӽ���Ĥ������ȫ�����˷�Ӧ�����װ�������ɵ���ȩ��Ϊ1.5mol���ʴ�Ϊ��1.5��
���� ���⿼�黯ѧƽ���йؼ��㡢��ѧƽ��Ӱ���ƶ�����˹���ɵ�֪ʶ�㣬���ؿ���ѧ���������㼰��ȡ��Ϣ��������������ѵ��ǣ�3����ƽ�ⳣ���ļ��㣬ע���ѹ�ļ��㷽������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A |  | 1��5-����-3-�һ��� |
| B |  | �����ϩ |
| C |  | 2��5-����-5-���� |
| D | CH3 CH2CH2��C2H5��CHCH��CH3��2 | 2-��-3-���������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
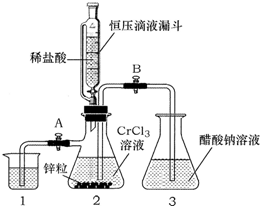 �����Ǹ�������һ���������ռ�����ѧʽΪ[Cr��CH3COO��2]2•2H2O����������ˮ�����������ᣮ����Cr2+�ױ������������Ʊ������Ǹ�ʱ�����ڷ����ϵ����п����ԭ�����Ƚ�Cr3+��ԭΪCr2+�������������Һ�����Ƶã����ܷ�ӦΪ��
�����Ǹ�������һ���������ռ�����ѧʽΪ[Cr��CH3COO��2]2•2H2O����������ˮ�����������ᣮ����Cr2+�ױ������������Ʊ������Ǹ�ʱ�����ڷ����ϵ����п����ԭ�����Ƚ�Cr3+��ԭΪCr2+�������������Һ�����Ƶã����ܷ�ӦΪ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 | B�� | 3 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
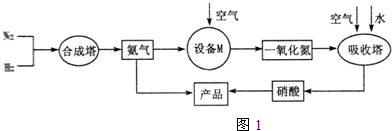
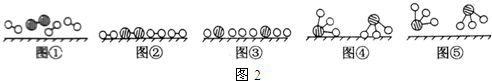
�� �ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ���N2��H2�������ڴ������桢�ڴ�������N2��H2�еĻ�ѧ�����ѣ�
�ֱ��ʾN2��H2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں�ͼ�۵ĺ���ֱ���N2��H2�������ڴ������桢�ڴ�������N2��H2�еĻ�ѧ�����ѣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
 �� |  �� |  �� |  �� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
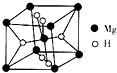 �������ʹ���������������õ���Ҫ�о�����
�������ʹ���������������õ���Ҫ�о������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com