
【题目】葡萄糖酸亚铁(C6H11O7) 2Fe是常用的补铁剂,易溶于水。用下图装置制备 FeCO3,提取出的 FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

Ⅰ.(1)如何检验 A 装置的气密性?____。
(2)B中加入药品Na2CO3,要使A中制得的FeSO4溶液进入B中发生反应,实验开始时,应打开分液漏斗的活塞、______,关闭_____,一段时间后,关闭_______,打开_____(填旋塞的编号)。
(3)将制得的碳酸亚铁悬浊液过滤、洗涤。如何证明沉淀已经洗涤干净_________。
(4)将葡萄糖酸与碳酸亚铁混合,反应的化学方程式为(有机物用分子式表示)_____。
(5)从环境保护的角度分析,该装置存在不足之处,请写出改正措施__________。
Ⅱ.某补铁剂的主要成分是硫酸亚铁,用氧化还原滴定法可测定该补铁剂中铁元素的含量,实验的主要步骤如下:
①取10片补铁剂样品,溶解除去不溶物(不损耗铁元素),并配成100mL待测溶液。
②量取20.00mL待测液于锥形瓶中。
③用cmol·L1的酸性KMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积,重复两次实验,平均消耗KMnO4溶液体积为VmL。
(6)上述实验中应该用稀硫酸酸化KMnO4溶液,如果用硝酸对KMnO4溶液进行酸化,对测定结果的影响是_____(填“偏大”“偏小”或“无影响”)。滴定终点的实验现象为_____。
(7)每片补铁剂含铁元素的质量为________________g(用代数式表示)。
【答案】关闭 K1、K2,打开分液漏斗的活塞,从分液漏斗上方注入水,若一段时间后,水不再滴下,且维持一段时间,则A装置的气密性良好,反之,则气密性不好 K2 K1 K2 K1 取少量最后一次洗涤液于一洁净的试管中,加入稀盐酸,无现象,再加入少量 BaCl2溶液,若无白色沉淀产生,则沉淀已经洗涤干净,反之,则未洗涤干净 2C6H12O7+FeCO3→(C6H11O7)2Fe+CO2+H2O 把尾气用酒精灯点燃 偏小 当滴入最后一滴酸性 KMnO4溶液时,溶液变为紫色,并且半分钟内不褪色,则达到滴定终点 0.14cv
【解析】
由实验装置图可知,该实验的反应为实验开始时,应打开分液漏斗的活塞、K2,关闭K1,装置A中铁屑与稀硫酸反应生成硫酸亚铁和氢气,利用反应生成的氢气将装置中的空气排尽,防止FeCO3被氧化,待空气排尽后,关闭K2,打开K1,反应生成的氢气使圆底烧瓶中压强增大,从而将A中生成的硫酸亚铁溶液压入装置B中,硫酸亚铁与碳酸钠反应生成碳酸亚铁沉淀,提取出的 FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。
(1)检验 A 装置的气密性可用液压法,具体操作为关闭 K1、K2,打开分液漏斗的活塞,从分液漏斗上方注入水形成密闭系统,若装置的气密性良好,加入水一段时间后,容器中气体压强增大,水不再滴下,且维持一段时间,故答案为:关闭 K1、K2,打开分液漏斗的活塞,从分液漏斗上方注入水,若一段时间后,水不再滴下,且维持一段时间,则A装置的气密性良好,反之,则气密性不好;
(2)B中加入药品Na2CO3,要使A中制得的FeSO4溶液进入B中发生反应,实验开始时,应打开分液漏斗的活塞、K2,关闭K1,装置A中铁屑与稀硫酸反应生成硫酸亚铁和氢气,利用反应生成的氢气将装置中的空气排尽,一段时间后,关闭K2,打开K1,反应生成的氢气使圆底烧瓶中压强增大,从而将A中生成的硫酸亚铁溶液压入装置B中,故答案为:K2;K1K2;K1;
(3)装置B中硫酸亚铁溶液与碳酸钠溶液反应生成碳酸亚铁沉淀和硫酸钠,过滤得到的碳酸亚铁表面附有可溶的硫酸钠,证明沉淀已经洗涤干净的标志是洗涤液中不含有硫酸钠,检验洗涤液中是否存在硫酸根离子可以选用酸化的氯化钡溶液,具体操作为取少量最后一次洗涤液于一洁净的试管中,加入稀盐酸,无现象,再加入少量 BaCl2溶液,若无白色沉淀产生,则沉淀已经洗涤干净,反之,则未洗涤干净,故答案为:取少量最后一次洗涤液于一洁净的试管中,加入稀盐酸,无现象,再加入少量 BaCl2溶液,若无白色沉淀产生,则沉淀已经洗涤干净,反之,则未洗涤干净;
(4)葡萄糖酸与碳酸亚铁反应生成葡萄糖酸亚铁、二氧化碳和水,反应的化学方程式为2C6H12O7+FeCO3→(C6H11O7)2Fe+CO2↑+H2O,故答案为:2C6H12O7+FeCO3→(C6H11O7)2Fe+CO2↑+H2O;
(5)从环境保护的角度来看,实验过程中的氢气没有处理,应选用气球收集或用酒精灯点燃处理氢气,故答案为:用酒精灯点燃;
(6)硝酸具有强氧化性,能将亚铁离子氧化,如果用硝酸对KMnO4溶液进行酸化,硝酸会氧化亚铁离子,导致与亚铁离子反应的酸性高锰酸钾的体积偏小,所测结果偏低;当溶液中的亚铁离子被完全氧化后,若再滴入酸性高锰酸钾溶液,溶液会变为紫色,故答案为:偏小;当滴入最后一滴酸性 KMnO4溶液时,溶液变为紫色,并且半分钟内不褪色,则达到滴定终点;
(7)溶液中亚铁离子与酸性高锰酸钾溶液发生氧化还原反应生成铁离子、锰离子和水,反应的离子方程式为MnO4-+ 5Fe2++8H+=Mn2++5Fe3++4H2O,反应中消耗KMnO4的物质的量为10-3cvmol,由方程式可知10片补铁剂样品中亚铁离子的物质的量为10-3cvmol×5×5=0.025 cvmol,则每片补铁剂含铁元素的质量为![]() =0.14cvg,故答案为:0.14cv。
=0.14cvg,故答案为:0.14cv。


科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.关于该电池的叙述正确的是( )

A. b极发生氧化反应
B. a极为该电池的正极
C. 放电时,电流从a极经过负载流向b极
D. a极的反应式:N2H4+4OH﹣﹣4e﹣═N2↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某石油化工产品X的转化关系如图,下列判断不正确的是( )
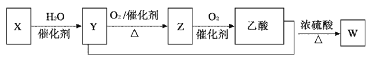
A. X可以发生加聚反应B. Y能与钠反应产生氢气
C. Z与CH3OCH3互为同分异构体D. W的结构简式为CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂采用如图装置处理化石燃料开采、加工过程产生的H2S废气,已知电解池中的两个电极均为惰性电极。下列说法不正确的是
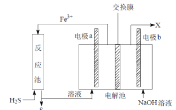
A.若交换膜为质子交换膜,则NaOH溶液的浓度逐渐变大,需要定期更换
B.若交换膜为阳离子交换膜,b 电极区会产生红褐色沉淀
C.电极 a 为阳极
D.反应池中处理H2S的反应是H2S +2Fe3+ = 2Fe2+ +S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
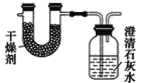
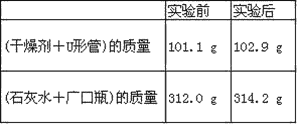
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为_____________g。
(2)生成的水中氢元素的质量为_______g。
(3)生成的二氧化碳中碳元素的质量为_______ g。
(4)该燃料中碳元素与氢元素的质量比为_______。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为_______,结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应方程式不正确的是
A.用Cl2与石灰制取漂白粉:2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
B.工业上用焦碳与石英砂制粗硅:SiO2+C![]() Si+CO2
Si+CO2
C.高温下铁与水蒸汽反应:3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
D.小苏打溶液与少量石灰水反应:2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列有关问题:
(1)现有下列有机物:
a.C(CH3)4 b.CH3CH2CH2CH3 c.CH3CH2COOH d.HCOOC2H5
①互为同分异构体的是________(填写有关序号,下同);
②互为同系物的是________;
③核磁共振氢谱只有一个峰(一种氢原子)的是________,按系统命名法该有机物的名称为________。
(2)下列五种物质中:①水、②乙醇、③醋酸、④苯酚、⑤碳酸。按羟基氢原子的活性由强到弱顺序排列正确的是(________)
A.③⑤④①② B.③④②①⑤ C.④①②⑤③ D.③②④①⑤
(3)乳酸的结构简式为: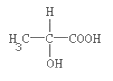 ,1mol乳酸最多可消耗NaOH的物质的量______,乳酸可以发生的反应有(填下列有关字母序号)_______。
,1mol乳酸最多可消耗NaOH的物质的量______,乳酸可以发生的反应有(填下列有关字母序号)_______。
a.酯化反应 b.加成反应 c.氧化反应 d.消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+CO(g)![]() CH3OH(g)为放热反应,对该反应的下列说法正确的是( )
CH3OH(g)为放热反应,对该反应的下列说法正确的是( )
A.因该反应为放热反应,故不加热就可发生
B.相同条件下,2 mol H2的能量或1 mol CO 的能量一定高于1 mol CH3OH的能量
C.相同条件下,反应物2 mol H2和1 mol CO 的总能量一定高于生成物1 mol CH3OH(g)的总能量
D.达到平衡时,CO的浓度与CH3OH的浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程的能量变化符合下图所示的是
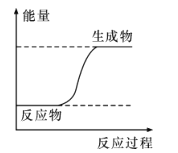
A. 酸碱中和反应
B. CH4在O2中燃烧
C. NH4Cl晶体与Ba(OH)28H2O晶体混合搅拌
D. CaO溶于水生成Ca(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com