
����Ŀ������Ҫ��ش������й����⣺
��1������������
a��C(CH3)4 b��CH3CH2CH2CH3 c��CH3CH2COOH d��HCOOC2H5
�ٻ�Ϊͬ���칹�����________����д�й���ţ���ͬ����
�ڻ�Ϊͬϵ�����________��
�ۺ˴Ź�������ֻ��һ���壨һ����ԭ�ӣ�����________����ϵͳ���������л��������Ϊ________��
��2���������������У���ˮ�����Ҵ����۴��ᡢ�ܱ��ӡ���̼�ᡣ���ǻ���ԭ�ӵĻ�����ǿ����˳��������ȷ������________��
A���ۢݢܢ٢� B���ۢܢڢ٢� C���ܢ٢ڢݢ� D���ۢڢܢ٢�
��3������Ľṹ��ʽΪ��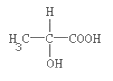 ��1mol������������NaOH�����ʵ���______��������Է����ķ�Ӧ�У��������й���ĸ��ţ�_______��
��1mol������������NaOH�����ʵ���______��������Է����ķ�Ӧ�У��������й���ĸ��ţ�_______��
a��������Ӧ b���ӳɷ�Ӧ c��������Ӧ d����ȥ��Ӧ
���𰸡�c��d a��b a 2��2-�������� A 1mol acd
��������
(1)�ٷ���ʽ��ͬ���ṹ��ͬ�Ļ����ﻥ��ͬ���칹�壻
�ڽṹ���ƣ��ڷ�����������һ����n��-CH2ԭ���ŵ��л��ﻥ��ͬϵ�
�۷����к��м�����ԭ�ӣ������շ���м���壻����ϵͳ������������
(2)���ʵ�����Խǿ��Խ������������ӣ����ǻ���ԭ�ӵĻ���Խǿ���ݴ˷�����
(3)�÷����к��д��ǻ����Ȼ������д�����������ʣ��ݴ˷������
(1)��c��d����ʽ��ͬ���ṹ��ͬ�����Ի���ͬ���칹�壬�ʴ�Ϊc��d��
��a��b�Ľṹ���ƣ��ڷ�����������1��-CH2ԭ���ţ�����ͬϵ��ʴ�Ϊa��b��
��ֻ��һ����ԭ�ӵ���a���������շ�ֻ��һ������a����������2��2-�������飻
(2)���ʵ�����Խǿ��Խ������������ӣ����ǻ���ԭ�ӵĻ���Խǿ�����ԣ����̼����ӣ�ˮ���Ҵ������ԣ�����������ӵ�����ˮǿ���Ҵ��������ǻ���ԭ�ӵĻ��ԴӴ�С˳���Ǣۢݢܢ٢ڣ��ʴ�ΪA��
(3)��ֻ���Ȼ��ܺ�NaOH��Ӧ����һ�����������ֻ��һ���Ȼ�������1mol������������NaOH�����ʵ��� 1mol��
�ڸ÷����к��д��ǻ����Ȼ������д�����������ʣ��ܷ���������Ӧ��������Ӧ����ȥ��Ӧ�������ܷ����ӳɷ�Ӧ����ѡacd��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ʳ���Ϳɻ��ij�����л�������X������Է�������Ϊ46������̼����������Ϊ52.2%�������������Ϊ13.0%���ṹ��������λ�ò�ͬ����ԭ�ӡ�
��1��X�ķ���ʽ��________������������________��
��2��X������Ʒ�Ӧ�ų���������Ӧ�Ļ�ѧ����ʽ��________________________��
��3��X������е�������ͭ�������·�Ӧ����Y��Y�Ľṹ��ʽ��________��X�����Ա����������Һֱ��������________����д���ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼�������̼���������ܵ���������Ĺ�ע�����������dz�����CO2���ϳɸ����л������������CO2�ϳ�һ�ֲ����������ķ�Ӧ����ʽ��

(1)д��CO2�Ľṹʽ__________����-R���Ľṹ��ʽΪ____________��
(2)������Ӧ�ķ�Ӧ����Ϊ_______����3����R-C��C-RҲ�ɷ������Ʒ�Ӧ���������л���Ľṹ��ʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������(C6H11O7) 2Fe�dz��õIJ�������������ˮ������ͼװ���Ʊ� FeCO3����ȡ���� FeCO3���������ᷴӦ�ɵ����������������ش��������⣺

��1����μ��� A װ�õ������ԣ�____��
��2��B�м���ҩƷNa2CO3��ҪʹA���Ƶõ�FeSO4��Һ����B�з�����Ӧ��ʵ�鿪ʼʱ��Ӧ��Һ©���Ļ�����______���ر�_____��һ��ʱ��ر�_______����_____���������ı�ţ���
��3�����Ƶõ�̼����������Һ���ˡ�ϴ�ӡ����֤�������Ѿ�ϴ�Ӹɾ�_________��
��4��������������̼��������ϣ���Ӧ�Ļ�ѧ����ʽΪ���л����÷���ʽ��ʾ��_____��
��5���ӻ��������ĽǶȷ�������װ�ô��ڲ���֮������д��������ʩ__________��
��ij����������Ҫ�ɷ���������������������ԭ�ζ����ɲⶨ�ò���������Ԫ�صĺ�����ʵ�����Ҫ�������£�
��ȡ10Ƭ��������Ʒ���ܽ��ȥ������������Ԫ�أ��������100mL������Һ��
����ȡ20.00mL����Һ����ƿ�С�
����cmol��L1������KMnO4��Һ�ζ����յ㣬��¼����KMnO4��Һ��������ظ�����ʵ�飬ƽ������KMnO4��Һ���ΪVmL��
��6������ʵ����Ӧ����ϡ�����ữKMnO4��Һ������������KMnO4��Һ�����ữ���Բⶨ�����Ӱ����_____������ƫ������ƫС��������Ӱ���������ζ��յ��ʵ������Ϊ_____��
��7��ÿƬ����������Ԫ�ص�����Ϊ________________g���ô���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� ( )
����������ͬ������һ������ͬ��Ԫ�� ��ͬλ�ص����������нϴ������ѧ���ʼ�����ȫ��ͬ ��Ԫ��������������������ԭ������������������������ͬ������Ԫ����Ҫ��ѧ�������������������� �ܵ�������ͬ�����Ӳ�һ����ͬһ��Ԫ�� ��ÿ��Ԫ�ض������ֻ������Եĺ���
A.�٢ڢܢ�B.�ۢܢ�C.�ڢۢ�D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���ɻ�ͭ��(��Ҫ�ɷ�Ϊ CuFeS2)ұ��ͭ����Ҫ�������¡�����˵������ȷ����
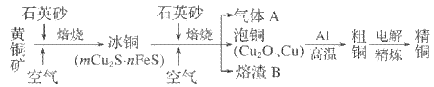
A. ����A�еĴ�����Ⱦ����ð�ˮ���ղ���������
B. ����ͭұ����ͭ�Ļ�ѧ����ʽΪ3Cu2O+2Al ![]() Al2O3+6Cu
Al2O3+6Cu
C. ����ʯӢɰ��Ϊ���Ӽ��ۼ������ɸ��ȶ�����������Ĺ�����
D. �ù���ϡH2SO4��ȫ���ܽ�����B
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijЩ���ʵ�ת��������ͼ��ʾ����x��y��z��������ͬ��һ��Ԫ�ء�ͼʾ���в���������δ�г���
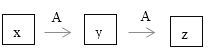
��1������x��AlCl3����y�Ļ�ѧʽ��________________
����x�������Ӻ�����Ԫ�أ�д������������������ᷴӦ�����ӷ���ʽ��___________________
��2����x��һ�ֻ���ɫ�ж��������壬A������ʹ��������һ�ֽ������ʡ�
��д��AԪ��ԭ�ӵĵ����Ų�ʽ��__________________
������y����Һ��һ�㲻�ǰ�Y�ľ�������ˮ�����ǰ�y�ľ������ܽ���_________���ѧʽ����Һ�С�
����μ���z�����е������ӣ�________________________________________________��
��3������x����ʹʪ���ɫʯ����ֽ���������壬�����������ԭ�ӹ���ӻ�������______________
�����и�����ϣ���������ͼ��Ӧ����______________������ţ�
�� x: N2 A: O2 �� x: Al A: NaOH �� x: Ba(OH)2 A: CO2
�� x: S A: O2 �� x: HNO3 A: Fe �� x: SiO2 A: C
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С����ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A(A�¶˻����ر�)�С�
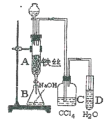
(1)д��A�з�Ӧ�Ļ�ѧ����ʽ_______________��
(2)�۲쵽A�е�������_____________________��
(3)ʵ�����ʱ����A�¶˵Ļ������÷�ӦҺ����B�У������Ŀ����________��д���йصĻ�ѧ����ʽ______________________________��
(4)C��ʢ��CCl4��������________________��
(5)��֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ�������Թ�D�м���AgNO3��Һ������������ɫ����������֤������һ����֤�ķ��������Թ�D�м���_______��������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�����У���ȷ����(����)
A.CCl4�ĵ���ʽΪ![]()
B.CaCl2�ĵ���ʽΪ![]()
C.HClO�ĽṹʽΪH��Cl��O
D.�õ���ʽ��ʾHCl���γɹ���Ϊ![]()
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com