
【题目】下列说法不正确的是 ( )
①质子数相同的粒子一定属于同种元素 ②同位素的物理性质有较大差别而化学性质几乎完全相同 ③元素种类由质子数决定,原子种类由质子数和中子数共同决定,元素主要化学性质由最外层电子数决定 ④电子数相同的粒子不一定是同一种元素 ⑤每种元素都有两种或两种以的核素
A.①②④⑤B.③④⑤C.②③⑤D.①⑤
科目:高中化学 来源: 题型:
【题目】人体吸入CO后在肺中发生反应CO+HbO2![]() O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )
O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )

A.反应开始至4s内用HbO2表示的平均反应速率为2×l0-4mol/(L·s)
B.反应达平衡之前,O2与HbCO的反应速率逐渐减小
C.将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D.该温度下反应CO+HbO2 ![]() O2+HbCO的平衡常数为107
O2+HbCO的平衡常数为107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、金属铋生产中,副产品 NaBiO3可作测定锰的氧化剂。工业上常用辉铋矿(主要成分是Bi2S3,还含有少量SiO2等杂质),制备BiOCl和NaBiO3(二者都难溶于水),其流程如下:
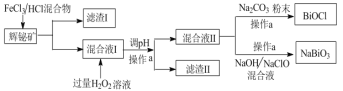
(1)操作a使用的玻璃仪器是_____________,工业上制备HCl的反应原理是:_____。
(2)滤渣I中的成分为________,分离滤渣I中的成分的物理方法是:__________。
(3)请从平衡角度解释调pH产生滤渣Ⅱ的原因:__。
(4)混合液 II 中加入 Na2CO3粉末,当混合液Ⅱ中____________(填实验现象)时,说明BiOCl的生成已完成。混合液II中加入NaOH和NaClO发生的离子方程式________。
(5)加入 H2O2发生反应的离子方程式_______,过滤后,如何洗涤BiOCl固体_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的O2中燃烧,并使产生的气体全部通过如图所示装置中,得到如表中所列的实验结果(假设产生的气体完全被吸收)。
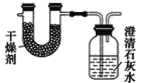
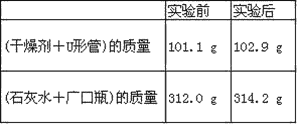
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为_____________g。
(2)生成的水中氢元素的质量为_______g。
(3)生成的二氧化碳中碳元素的质量为_______ g。
(4)该燃料中碳元素与氢元素的质量比为_______。
(5)已知这种燃料的每个分子中含有一个氧原子,则该燃料的分子式为_______,结构简式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋为第五周期VA族元素,利用湿法冶金从辉铋矿(含Bi2S3、Bi、Bi2O3等)提取金属铋的工艺流程如下图所示:
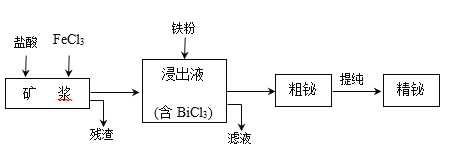
已知:BiCl3水解的离子方程式为:BiCl3+H2O![]() BiOCl+2H++2Cl。
BiOCl+2H++2Cl。
(1)矿浆浸出时加入盐酸的作用是____。
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为____。
(3)残渣中含有一种单质,该单质是_______。
(4)滤液的主要溶质是(化学式)_____,该物质可在工艺中转化为循环利用的原料,转化的反应方程式为____。
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以______(填化学式)进入残渣中。
(6)粗铋电解精炼时应放在_______极。
(7)某温度下饱和的Ag2S溶液中,银离子的浓度为10-4mol/L,且Ag2S的KSP=5.8×10-39,则此溶液中硫离子的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列有关问题:
(1)现有下列有机物:
a.C(CH3)4 b.CH3CH2CH2CH3 c.CH3CH2COOH d.HCOOC2H5
①互为同分异构体的是________(填写有关序号,下同);
②互为同系物的是________;
③核磁共振氢谱只有一个峰(一种氢原子)的是________,按系统命名法该有机物的名称为________。
(2)下列五种物质中:①水、②乙醇、③醋酸、④苯酚、⑤碳酸。按羟基氢原子的活性由强到弱顺序排列正确的是(________)
A.③⑤④①② B.③④②①⑤ C.④①②⑤③ D.③②④①⑤
(3)乳酸的结构简式为: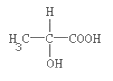 ,1mol乳酸最多可消耗NaOH的物质的量______,乳酸可以发生的反应有(填下列有关字母序号)_______。
,1mol乳酸最多可消耗NaOH的物质的量______,乳酸可以发生的反应有(填下列有关字母序号)_______。
a.酯化反应 b.加成反应 c.氧化反应 d.消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种有机物,它们的分子分别由—CH3、—OH、—COOH、—CHO、—C6H5( 代表苯基)中的两种组成,这些化合物的性质如下所述:
①A能够发生银镜反应,且相对分子质量为44;
②B溶液加入氯化铁溶液中,溶液显紫色;
③C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
④B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
⑤D属于烃类,且D能使酸性高锰酸钾溶液褪色,还能发生硝化反应。
请回答下列问题:
(1)B、D的结构简式是:B_____D______
(2)写出A发生银镜反应的化学方程式:________
(3)C和E发生酯化反应的化学方程式:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学设计了如图1装置,根据元素非金属性与对应最高价含氧酸之间的关系,可以一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、蘸有碱液的棉花。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
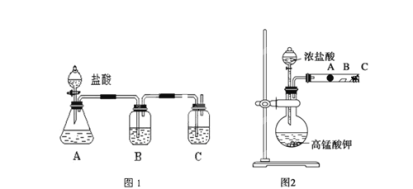
(1)根据实验图1作答:
①写出选用试剂分别 B__________,C____________
②装置B中所盛试剂的作用为_________
③C中反应的离子方程式为_______
④从实验所得非金属性C____Si(填“大于”或“小于”)
(2)根据实验图2作答:
①写出 A处的离子方程式:_______
②B处的现象_____
③C处药品的作用 _______。
④通过图2 装置实验得出同主族元素性质的递变规律为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据化学反应与热能的有关知识,填写下列空白:
(1)某同学做如下实验,以检验反应中的能量变化。
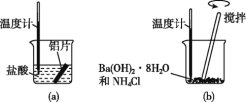
①在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是___热反应;(b)中温度降低,由此可以判断(b)中反应是___热反应。
②根据能量守恒定律,(b)中反应物的总能量应该__其生成物的总能量(填“>”或“<”)。
(2)下列过程中不一定放热的是______ (填字母)。
a.葡萄糖在体内的氧化 b.炸药爆炸 c.燃料燃烧 d.化合反应 e.酸碱中和
(3)已知H2和O2反应放热,且断开1 mol H-H键、1 mol O=O键、1 mol O-H键需吸收的能量分别为Q1 kJ、Q2 kJ、Q3 kJ,由此可以推知下列关系正确的是______ (填编号)。
①Q1+Q2>Q3 ②2Q1+Q2<4Q3 ③Q1+Q2<2Q3 ④2Q1+Q2>2Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com