
【题目】下列有关说法中正确的是
A. 乙烯的结构筒式可以表示为CH2CH2 B. 苯、乙醇和乙酸都能发生取代反应
C. 乙醇和乙酸都存在碳氧双键 D. 液化石油气和天然气的主要成分都是甲烷
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】目前海水液化可采用双极膜电液析法、同时获得副产品,其模拟工作原理如图所示。其中双极膜(BP)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-,作为H+和OH-离子源。M、N为离子交换膜。下列说法正确的是( )

A. X电极为电解池的阴极,该电极反应式为:2H+-2e-=H2↑
B. 电子流向:电源负极→X电极→Y电极→电源正极
C. 电路中每转移1mol电子,X、Y两极共得到标准状况下16.8L的气体
D. M为阳离子交换膜,A室获得副产品NaOH;若去掉B室双极膜,B室产物不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。
主反应:C4H10(g,正丁烷) ![]() C2H4(g)+C2H6(g)△H1
C2H4(g)+C2H6(g)△H1
副反应:C4H10 (g,正丁烷) ![]() CH4(g)+C3H6(g) △H2
CH4(g)+C3H6(g) △H2
回答下列问题:
(1)化学上,将稳定单质的能量定为0,生成稳定化合物时的释放或吸收能量生成热,生成热可表示该物质相对能量。下表为25℃、101kPa下几种有机物的生成热:
物质 | 曱烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
①表格中的物质,最稳定的是_________________(填结构简式)。
②上述反应中,△H1=______kJ/mol。
③书写热化学方程式时,要标明“同分异构体名称”,其理由是________________________。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况表明该反应达到平衡状态的是_______(填代号)。
A.气体密度保持不变 B.[c(C2H4)·c(C2H6)]/ c(C4H10)保持不变
C.反应热不变 D.正丁烷分解速率和乙烷消耗速率相等
②为了同时提高反应速率和转化率,下列措施可采用的是_____(填代号)。
A.加入高效催化剂B.升高温度C.充入乙烷D.减小压强
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随若温度升高,乙烯产率降低,可能的原因是__________(填代号)。

A.平衡常数降低 B.活化能降低C.催化剂活性降低 D.副产物增多
(4)在一定温度下向1L恒容密闭容器中充入2mol正丁烷,反应生成乙烯和乙烷,经过10min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10min内乙烯的生成速率v(C2H4)为________mol·L-1·min-1。
②上述条件下,该反应的平衡常数K为____________。
(5)丁烷-空气燃料电池以熔融的K2CO3为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的负极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+3B(g)4C(g)+D(g),已知起始浓度c(A)=4molmol﹣1 , c(B)=3molmol﹣1 , C、D浓度均等于0,反应开始2秒后达到平衡状态,此时D的平衡浓度为0.5molL﹣1 , 则下列说法不正确的是( )
A.反应速率v(C)=1molL﹣1s﹣1
B.C的平衡浓度为4 molL﹣1
C.A的转化率为25%
D.B的平衡浓度为1.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定温度下在2L的密闭容器内发生反应:H2(g)+I2(g)![]() 2HI(g),开始时通入0.8molH2和一定量的I2(g),各物质的浓度随时间的变化情况如图所示,其中I2(g)的浓度变化曲线前半部分已略去。
2HI(g),开始时通入0.8molH2和一定量的I2(g),各物质的浓度随时间的变化情况如图所示,其中I2(g)的浓度变化曲线前半部分已略去。

请回答下列问题:
(1)比较正反应速率(同一物质)的大小:A点_____(填“>”“≤”或“=”)B点。
(2)从反应开始至达到平衡,HI的平均反应速率为________。
(3)起始时I2的物质的量为______mol。
II.下图是煤综合利用的一种简单流程。已知烃A对氢气的相对密度是14,C为常见的酸味剂,E是一种有水果香味的透明液体。

(1)有机物D中含有的官能团的名称是___________。
(2)①~⑥过程中属于加成反应的是_______(填序号)。
(3)写出③的反应方程式____________。
(4)下列说法正确的是____(填字母)。
a.第①步是煤的液化,为煤的综合利用的一种方法
b.有机物C和D都可以与金属钠发生反应
c.有机物C和D的水溶液都具有杀菌消毒作用
d.有机物E与有机物D混合物的分离,可以用氢氧化钠溶液振荡、分液方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:

完成下列填空:
(1)焙烧产生的SO2可以继续制备硫酸,其中的反应之一为:2SO2+O2 ![]() 2SO3+Q(Q>0),该反应的平衡常数表达式为K=___________;欲使K值增大,可采取的措施是______________。若经一段时间后SO3的浓度增加了4mol/L,在这段时间内用O2表示的反应速率为0.4 mol/(Ls),则这段时间为_______(选填编号)。
2SO3+Q(Q>0),该反应的平衡常数表达式为K=___________;欲使K值增大,可采取的措施是______________。若经一段时间后SO3的浓度增加了4mol/L,在这段时间内用O2表示的反应速率为0.4 mol/(Ls),则这段时间为_______(选填编号)。
a.1s b.5s c.10s d.50s
(2)硫铁矿焙烧后的烧渣中含有Fe2O3、Fe3O4等。酸溶后溶液中主要存在的阳离子有______________,不能用硫酸代替盐酸的原因是____________________________。
(3)通入氯气时,主要反应的离子方程式为________________________。从氧化后的溶液中得到氯化铁晶体的实验步骤为_______________、_______________、过滤洗涤。
(4)酸溶及后续过程中均需保持盐酸过量,请从水解平衡移动原理解释原因_________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y、Z的分子式均为C7H8,结构简式如下:
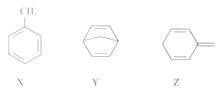
下列说法正确的是
A. X、Y、Z均为苯的同系物
B. X、Y、Z分子中的碳原子均处于同一平面
C. X、Y、Z均能使酸性高锰酸钾溶液褪色
D. 1molX、1molY分别与足量溴的四氯化碳溶液反应,均最多消耗2mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钾可用于有机合成、制药等领域,它是一种白色立方结晶或粉末,易溶于水。有两个学习小组查阅资料后,分别设计以下实验装置制备KI:
【查阅资料】:
(1)3I2+6KOH═KIO3+5KI+3H2O
(2)H2S是有剧毒的酸性气体,具有较强还原性,水溶液称氢硫酸(弱酸);
(3)HCOOH(甲酸)具有强烈刺激性气味的液体,具有较强还原性,弱酸;
(4)在实验条件下,S2-、HCOOH分别被KIO3氧化为SO42-、CO2。
Ⅰ组. H2S还原法,实验装置如图:

实验步骤如下:
①在上图所示的C中加入127g研细的单质I2和210g 30%的KOH 溶液,搅拌至碘完全溶解。
②打开弹簧夹向其中通入足量的 H2S。
③将装置C中所得溶液用稀H2SO4酸化后,置于水浴上加热10min。
④在装置C的溶液中加入BaCO3,充分搅拌后,过滤、洗涤。
⑤将滤液用氢碘酸酸化,将所得溶液蒸发浓缩,冷却结晶、过滤、洗涤、干燥。得产品145g。
Ⅱ组.甲酸还原法,实验装置如图:

实验步骤如下:
⑥在三颈瓶中加入 127g 研细的单质I2和210g 30%的 KOH 溶液,搅拌至碘完全溶解。
⑦通过滴液漏斗向反应后的溶液中滴加入适量HCOOH,充分反应后,再用KOH溶液调pH至9~10,将所得溶液蒸发浓缩,冷却结晶、过滤、洗涤、干燥。得产品 155g。
回答下列问题;
(1)图中装置 A 中发生反应的离子方程式为__________;装置 B 中的试剂是_________。
(2)D装置的作用是___________。
(3)步骤④的目的是_____________________ 。
(4)步骤⑤中“滤液用氢碘酸酸化”的目的是__________________ 。
(5)Ⅱ组实验的产率为__________________。
(6)Ⅱ组实验中,加入HCOOH发生氧化还原反应的离子方程式为_______________。
(7)与Ⅰ组相比较,Ⅱ组实验的优点是(至少答出两点即可)__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com