
【题目】目前海水液化可采用双极膜电液析法、同时获得副产品,其模拟工作原理如图所示。其中双极膜(BP)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-,作为H+和OH-离子源。M、N为离子交换膜。下列说法正确的是( )

A. X电极为电解池的阴极,该电极反应式为:2H+-2e-=H2↑
B. 电子流向:电源负极→X电极→Y电极→电源正极
C. 电路中每转移1mol电子,X、Y两极共得到标准状况下16.8L的气体
D. M为阳离子交换膜,A室获得副产品NaOH;若去掉B室双极膜,B室产物不变
【答案】C
【解析】A、电解池中阳离子向阴极移动,故X电极为阴极,电极反应式为:2H++2e-=H2↑,选项A错误;B. 电子流向:电源负极→阴极X电极、阳极Y电极→电源正极,选项B错误;C、阴极反应为2H++2e-=H2↑,阳极反应为:4OH--4e-=O2↑+2H2O,当电路中通过1mol电子时,阴极得到0.5molH2,阳极得到0.25molO2,两极一共得到气体为0.5mol+0.25mol=0.75mol,标准状况下16.8L的气体,选项C正确;D、电解池中,电解时,溶液中的阳离子向阴极移动,阴离子向阳极移动,因此M为阳离子交换膜,A室获得副产品NaOH;若去掉双极膜(BP),则Cl-会在阳极失去电子,生成Cl2,在阳极室会有C12生成,,B室产物发生变化,选项D错误。答案选C。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】工业上电解食盐水的原理是:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。成品碱中含有氯化钠杂质,可通过分光光度法测定每克成品碱中氯化钠的含量,其测量值(吸光度A)与每克成品碱中氯化钠含量的关系如下图,氯化钠杂质小于0.0050%的成品碱为优品级。下列说法不正确的是
2NaOH+H2↑+Cl2↑。成品碱中含有氯化钠杂质,可通过分光光度法测定每克成品碱中氯化钠的含量,其测量值(吸光度A)与每克成品碱中氯化钠含量的关系如下图,氯化钠杂质小于0.0050%的成品碱为优品级。下列说法不正确的是

A. 吸光度A的值越大,样品中氯化钠含量越小
B. 分光光度法是对物质组成进行定性和定量的测定
C. 图中G点所测的成品碱不是优品级
D. 成品碱是否含有NaCl,可用硝酸酸化的硝酸银溶液检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示下列描述正确的是
A.反应开始到10s,用Z表示的反应速率为0.158 mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C.反应开始到10s,Y的转化率为79.0 %
D.反应的化学方程式为:X+Y ![]() Z
Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
B. 1mol硝基(-NO2)与46g二氧化氮所含的电子数均为23NA
C. 16.2g14C10H22中含有的共价键数目为3.2NA
D. 向含1molFeI2的溶液中通入1molCl2充分反应,该反应转移电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的操作、现象及实验原理或结论均正确的是( )
实验目的 | 操作和现象 | 实验原理或结论 | |
A | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 向1mLlmol·L-1MgCl2溶液中滴加2滴2mol·L-1NaOH溶液,生成白色沉淀;再滴加2滴1mol·L-1'FeCl3溶液,白色沉淀变成红褐色沉淀 | 3Mg(OH)2(s)+2Fe3+(aq) |
B | 比较HClO和CH3COOH的酸性 | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 酸越弱,酸根离子水解程度越大,其盐溶液碱性越强 |
C | 提纯混有少量硝酸钾的氯化钠固体 | 在较高温度下制得浓溶液再冷却结晶、过滤、干燥 | 氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大 |
D | 检验某溶液中是否含有SO42- | 向该溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用方铅矿精矿(主要为PbS)和软锰矿(主要为MnO2,还有少量Fe2O3,Al2O3等杂质)制备PbSO4和Mn3O4的工艺流程如下:

已知:①PbS+MnO2+4H+=Mn2++Pb2++S+2H2O
②25℃时,Ksp(PbCl2)=1.6×10-5,Ksp(PbSO4)=1.8×10-8
③PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
(1)80℃用盐酸处理两种矿石,为加快酸浸速率,还可采用的方法是_______________(任写一种)。
(2)向酸浸液中加入饱和食盐水的目的是_________________;加入物质X可用于调节酸浸液的pH值,物质X可以是___________(填字母)。
A.MnCO3 B.NaOH C.ZnO D.PbO
(3)滤渣中含有两种金属杂质形成的化合物,其成分为_____________(写化学式);
请设计分离两种金属化合物的路线图(用化学式表示物质,用箭头表示转化关系,箭头上注明试剂和分离方法)。______________________________________
(4)向滤液2中通入NH3和O2发生反应,写出总反应的离子方程式。___________________________________
(5)用Mn3O4为原料可以获得金属锰,选择合适的冶炼方法为___________(填字母)。
A.热还原法 B.电解法 C.热分解法
(6)求25℃氯化铅沉淀转化为硫酸铅沉淀反应的平衡常数K=___________(保留到整数位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钛、镍等过渡元素在工业生产和科学研究中具有重要作用,请回答下列问题。
(1)有机铁肥[Fe(H2NCONH2)6](NO3)3的名称叫三硝酸六尿素合铁,是一种配合物,它的中心离子Fe3+的价电子排布式为____________;该配合物中N原子的杂化方式有_______________;它所含非金属元素的电负性由小到大的顺序是__________________。
(2)钛被称为继铁、铝之后的“第三金属”,也叫“未来金属”。
①钛位于周期表的_______区,基态Ti原子的电子占据了____________个原子轨道。
②工业上可用TiCl4(常温下呈液态)与Mg高温下反应制备钛单质,同时生成MgCl2,详细解释TiCl4熔点比MgCl2低很多的原因 _______________________________________________________ 。
(3)镍与CO生成的配合物Ni(CO)4中,易提供孤电子对的成键原子是_______________(填元素名称);1molNi(CO)4中含有的σ键数目为_________________ ;写出与CO互为等电子体的一种离子的化学式___________。
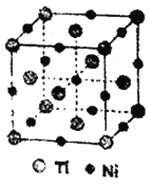
(4)镍钛记忆合金用于飞机和字宙飞船。已知一种钛镍合金的晶胞结构如图所示,其中Ti原子采用面心立方最密堆积方式,该合金中与Ti原子距离最近且相等的Ni原子个数为________;若合金的密度为ρg/cm3,NA代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是____________pm。(用含ρ和NA的计算式表示,不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.由H原子形成1molH﹣H键要吸收热量
B.所有燃烧反应都是放热反应
C.在稀溶液中,1mol酸与1mol碱发生中和反应生成水时所释放的热量称为中和热
D.凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是
A. 乙烯的结构筒式可以表示为CH2CH2 B. 苯、乙醇和乙酸都能发生取代反应
C. 乙醇和乙酸都存在碳氧双键 D. 液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com