
【题目】为加速漂粉精的消毒作用,最好的方法是
A.用水溶解B.加入少量稀盐酸C.干燥后使用D.加入NaOH溶液
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的四种短周期元素,A2﹣和B+具有相同的电子构型,C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子. 回答下列问题:
(1)C原子的核外电子排布式为 .
(2)单质A有两种同素异形体,其中沸点高的是(填分子式),原因是;A、B、D三元素组成的化合物所属的晶体类型是 .
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为 , 中心原子的杂化轨道类型为 .
(4)A和B能够形成化合物1:1的化合物,写出此化合物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一.在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac. 请回答下列问题:
(1)C,N,O的第一电离能由大到小的顺序为 .
(2)写出基态Cu+的核外电子排布式 .
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的离子: . (任写一个)
(5)某化合物的晶胞如图所示,写出该化合物的化学式 , 距离每个X+最近的Cl﹣的个数为 . 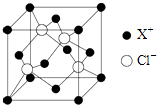
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A.2H2(g)+O2(g)═2H2O(1)△H=﹣285.8kJ/mol
B.2H2(g)+O2(g)═2H2O(1)△H=+571.6kJ/mol
C.2H2(g)+O2(g)═2H2O(g)△H=﹣571.6kJ/mol
D.H2(g)+ ![]() O2(g)═H2O(1)△H=﹣285.8kJ/mol
O2(g)═H2O(1)△H=﹣285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是自然賜给人类的宝藏,海水的综合利用是全世界研究的重点。
完成下列问题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO42-等杂质,粗盐获得精盐一般步骤:

加入氯化钡、纯碱和烧碱的目的依次是:_________、_________、_________。
(2)海水提取金属镁流程如下:

流程中加入熟石灰目的__________;沉淀与盐酸反应的离子方程式_____________。
(3)某学生实验室模拟河水提取溴的步骤为:海水→浓缩→氧化→提取→溴
①氧化步骤:适宣作氧化剂的是_______。
ABr2 B.Cl2 C.I2 DHCl
②提取步骤:……溴水中加入CCl4振荡、静置……得溴的四氯化碳溶液,该分离提纯溴的方法叫________;用到的主要仪器为________。
(4)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: ________;Cu与硫磺反应的化学方程式________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温容器中加入1molN2和3molH2 , 达到平衡时NH3的体积分数为m%.若N2、H2、NH3的起始加入量分别为xmol、ymol、zmol,达到平衡时NH3的体积分数仍为m%.
(1)该容器恒容,则x、y、z应满足的关系是 .
(2)该容器恒压,则x、y、z应满足的关系是 .
(3)设前者达到平衡时生成NH3为amol,则后者达到平衡时生成NH3=mol(用a、x、z表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.一定量的CO(g)和H2O(g)分别通入容积为1L的恒容密闭容器中,发生反应CO(g)+H2OCO2(g)+H2(g)得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衝所需时间/min | |
CO | H2O | CO2 | |||
1 | 500 | 8 | 4 | 3.2 | 4 |
2 | 700 | 4 | 2 | 0.8 | 3 |
3 | 700 | 4 | 2 | 0.8 | 1 |
(1)①下列情况表明反应达到平衡状态的是 (填序号)
A.CO2和H2生成速率相等
B.温度不变时,压强不变
C.生成CO2的速率和生成CO的速率相等
②实验2中,反应达到平衡状态时,CO的转化率为 .
③实验3和实验2相比,改变的条件是 .
(2)①硫化钠溶液具有较强碱性,其原因是(用离子方程式表示).
②欲使0.1mol的Na2S溶液中, ![]() 的值增大,可采取的措施是(填序号)
的值增大,可采取的措施是(填序号)
A.加适量等浓度的NaOH溶液
B.加适量的水
C.通入适量的H2S气体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。

请回答下列问题:
(1)写出下列物质的化学式:B_________,丙_________,乙_________,H_________
(2)根据要求回答:
1)D溶液和F溶液在空气中混合的现象:_________________________________;
2)反应③离子方程式___________________________________________________;
3)反应⑦离子方程式___________________________________________________;
4)反应⑥化学方程式___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL 0.1molL﹣1NaOH溶液中加入0.1molL﹣1的一元酸HA溶液pH的变化曲线如图所示.下列说法不正确的是( ) 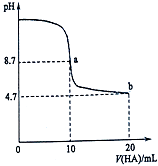
A.在逐滴加入HA溶液至20mL时,NaOH溶液中水的电离程度先增大后减小
B.b点所示溶液中c(A﹣)>c(HA)
C.pH=7时,c(Na+)=c(A﹣)+c(HA)
D.该酸是弱酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com