
【题目】25℃时,将氨水与氯化铵溶液混合得到c(NH3·H2O)+c(NH4+)=0.l mol·L-1的溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如下图所示。下列有关离子浓度关系叙述一定正确的是( )
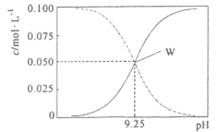
A.W点表示溶液中:c(NH3·H2O)+c(H+)=c(Cl-)+c(OH-)
B.pH=7.0溶液中: c(NH3·H2O)>c(NH4+)>c(OH-)=c(H+)
C.pH=10.5的溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1 mol·L-1
D.向W点所表示的1 L溶液中加入0.05 mol NaOH固体(忽略溶液体积变化):c(Na+)>c(Cl-)>c(OH-)>c(NH4+)
【答案】AD
【解析】
将氨水与氯化铵溶液混合得到c(NH3·H2O)+c(NH4+)=0.l mol/L的混合溶液,当溶液中只有NH4+时,NH4+水解使溶液呈酸性,随着c(NH3·H2O)的增大,溶液碱性增强,根据图示,当pH=9.25时,c(NH3·H2O)=c(NH4+),因此当溶液的pH<9.25时,c(NH3·H2O)<c(NH4+),当pH>9.25时,c(NH3·H2O)>c(NH4+),因此随着溶液pH的增大,浓度增大的是c(NH3·H2O)、减小的是c(NH4+)。
A.任何电解质溶液中都存在电荷守恒,根据电荷守恒可得c(Cl-)+c(OH-)=c(NH4+)+c(H+),在W点时c(NH3·H2O)=c(NH4+),所以c(NH3·H2O)+c(H+)=c(Cl-)+c(OH-),A正确;
B.室温下pH=7.0<9.25,溶液显中性,c(H+)=c(OH-),则溶液中c(NH4+)>c(NH3·H2O),NH3·H2O主要以电解质分子存在,NH3·H2O、H2O的电离程度十分微弱,其电离产生的离子浓度很小,故微粒浓度大小关系为:c(NH4+)>c(NH3·H2O)>c(H+)=c(OH-),B错误;
C.该混合溶液中,无论pH如何变化都存在c(Cl-)+c(OH-)=c(NH4+)+c(H+),则c(Cl-)+c(OH-)+c(NH3·H2O)=c(NH4+)+c(H+)+c(NH3·H2O)=0.1 mol/L+c(H+)>0.1 mol/L,C错误;
D.W点溶液中存在c(NH3·H2O)=c(NH4+)=0.05 mol/L,溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒可知c(Cl-)<c(NH4+)=0.05 mol/L,向1 L该溶液中加入0.05 mol NaOH,则c(Na+)=0.05 mol/L, c(Na+)>c(Cl-),NaCl电离产生离子浓度Cl-浓度c(Cl-)大于NH3·H2O电离产生的离子NH4+、OH-的浓度,且溶液中还有水会微弱电离产生OH-,故离子浓度关系为:c(Na+)>c(Cl-)>c(OH-)>c(NH4+),D正确;
故合理选项是AD。


科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值.下列说法正确的是( )
A.46g乙醇中存在的共价键总数为7NA
B.HNO3作为氧化剂得到的电子数一定为3NA
C.1mol甲醇完全燃烧时,转移的电子数为6NA
D.将3.4g H2S全部溶于水,所得溶液中HS-和S2-离子数之和为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下两个容积相等的储气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混合气体,两瓶气体一定具有相同的( )
A.质量B.密度C.碳原子数D.原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法不正确的是( )
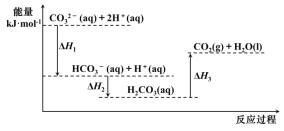
A.反应![]() (aq)+H+(aq)═CO2(g)+H2O(l) △H>0
(aq)+H+(aq)═CO2(g)+H2O(l) △H>0
B.![]() (aq)+2H+(aq)═CO2(g)+H2O(l) △H=△H1+△H2+△H3
(aq)+2H+(aq)═CO2(g)+H2O(l) △H=△H1+△H2+△H3
C.△H1>△H2,△H2<△H3
D.H2CO3(aq)═CO2(g)+H2O(l),若使用催化剂,则△H3不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3和NaHCO3在生活和生产中应用广泛。
(1)室温时下列指定溶液中微粒物质的量浓度关系正确的是_____ (填字母) .
A.0.1mol·L-1的Na2CO3溶液: c(Na+)+c(H+) =c(OH-)+c(![]() )+c(
)+c(![]() )
)
B.0.1mol·L-1的NaHCO3溶液: c(Na+) =c(![]() ) + c(
) + c(![]() )+ c(H2CO3)
)+ c(H2CO3)
C.0.1mol·L-1的NaHCO3溶液: c(Na+)>c(![]() )>c(
)>c(![]() )>c(H2CO3)
)>c(H2CO3)
D.浓度均为0.1mol·L-1的Na2CO3和NaHCO3混合溶液:2c(H+)+c(![]() )+3c(H2CO3)=2c(OH-)+c(
)+3c(H2CO3)=2c(OH-)+c(![]() )
)
(2)水垢中的CaSO4可用Na2CO3溶液处理。当两种沉淀共存时,  =________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
=________;[Ksp(CaCO3) =5.0×10-9、Ksp(CaSO4)=7.0×10-5]
(3) 25℃时,碳酸及其盐溶液中含碳元素微粒的分布分数δ随溶液pH变化的关系如图所示。
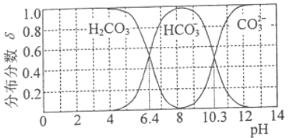
①纯碱溶液去油污的原理是_________(用离子方程式表示) 。25℃时,该反应的平衡常数表示为Kh,则pKh=_________(pKh=-lgKh)。
②25C时,下列三种溶液
A.0.1mol·L-1的NaHCO3溶液:
B.0.1mol·L-1的Na2CO3溶液:
C.0.1mol·L-1的NaCN溶液。
pH由大到小的顺序为________________(填字母)。[25℃时,K(HCN)= 10-9.3]
(4)NaHCO3可用于铝土矿(主要成分为Al2O3,含SiO2和Fe2O3)制铝。流程如下:
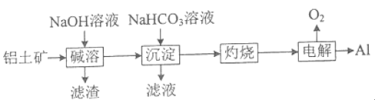
①滤渣中除含SiO2转化得到的铝硅酸钠外,还含_____(填化学式) 。
②写出“沉淀"步骤发生反应的离子方程式________和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PMMA骨水泥的成分为聚甲基丙烯酸甲酯,结构简式为 ,其单体丙的制备原理如图所示,下列说法中错误的是
,其单体丙的制备原理如图所示,下列说法中错误的是

A.丙所含的官能团有碳碳双键、酯基
B.可以用饱和碳酸氢钠溶液鉴别甲、乙、丙
C.丙与聚甲基丙烯酸甲酯互为同系物
D.甲+乙→丙的反应类型为取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com