
【题目】向Na2CO3溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法不正确的是( )
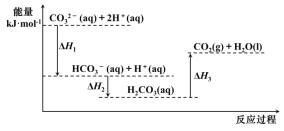
A.反应![]() (aq)+H+(aq)═CO2(g)+H2O(l) △H>0
(aq)+H+(aq)═CO2(g)+H2O(l) △H>0
B.![]() (aq)+2H+(aq)═CO2(g)+H2O(l) △H=△H1+△H2+△H3
(aq)+2H+(aq)═CO2(g)+H2O(l) △H=△H1+△H2+△H3
C.△H1>△H2,△H2<△H3
D.H2CO3(aq)═CO2(g)+H2O(l),若使用催化剂,则△H3不变
【答案】C
【解析】
由图可知,![]() (aq)+2H+(aq)生成
(aq)+2H+(aq)生成![]() (aq)+H+(aq)以及
(aq)+H+(aq)以及![]() (aq)+H+(aq)生成H2CO3(aq)都为放热反应,H2CO3(aq)生成CO2(g)+H2O(l)为吸热反应,结合图象中能量的高低分析解答。
(aq)+H+(aq)生成H2CO3(aq)都为放热反应,H2CO3(aq)生成CO2(g)+H2O(l)为吸热反应,结合图象中能量的高低分析解答。
A.由图可知反应![]() (aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应,△H>0,故A正确;
(aq)+H+(aq)=CO2(g)+H2O(l)为吸热反应,△H>0,故A正确;
B.由盖斯定律可知![]() (aq)+2H+(aq)=CO2(g)+H2O(l) △H=(△H1+△H2+△H3),故B正确;
(aq)+2H+(aq)=CO2(g)+H2O(l) △H=(△H1+△H2+△H3),故B正确;
C.由图可知,能量差值越大,反应热的绝对值越大,△H1、△H2都为放热反应,则△H1<△H2,故C错误;
D.加入催化剂,改变反应历程,但反应热不变,故D正确;
故选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.H2(g)的燃烧热△H=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g) △H=+571.6 kJ/mol
B.反应物的总能量低于生成物的总能量时,该反应为放热反应
C.由石墨比金刚石稳定可知:c(金刚石,s)=c(石墨,s) △H<0
D.已知:298K时,N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
2NH3(g) △H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入0.5 mol N2和1.5mol H2,达到平衡时放出46.0 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 的结构简式如下:下列有关M 叙述不正确的是( )
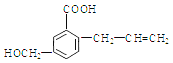
A. M的分子式为C11H12O3
B. 能使溴的四氯化碳溶液褪色
C. 一定条件下,M能生成高分子化合物
D. 能发生加成反应不能发生取代反应
【答案】D
【解析】
试题A.根据物质的结构简式可知M的分子式是C11H12O3,正确; B.该物质的分子中含有碳碳双键,因此能使溴的四氯化碳溶液褪色,正确;C. 该物质的分子中含有碳碳双键,在一定条件下发生加聚反应形成高聚物,正确;D. 化合物M含有碳碳双键,因此能发生加成反应,含有醇羟基、羧基,因此可以发生取代反应,错误。
考点:考查有机物的结构与性质的关系的知识。
【题型】单选题
【结束】
22
【题目】下列有关金属腐蚀与防护的说法不正确的是( )
A. 钢铁发生电化学腐蚀时,若表面水膜呈中性,则正极发生的反应为:2H2O+O2+4e一= 4OH一
B. 在潮湿的空气中,黄铜(铜锌合金)制品比纯铜制品更易产生铜绿
C. 金属制品在海水中比淡水中更容易发生腐蚀
D. 从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程
【答案】B
【解析】A、钢铁发生电化学腐蚀时,若表面水膜呈中性发生吸氧腐蚀,则正极发生的反应为:2H2O+O2+4e一=4OH一,A正确;B、在潮湿的空气中易发生电化学腐蚀,锌的金属性强于铜,因此黄铜(铜锌合金)制品比纯铜制品更不易产生铜绿,B错误;C、海水中含电解质浓度大,淡水中含电解质浓度小,故金属制品在海水中比淡水中更容易发生腐蚀,C正确;D、从本质上看,金属腐蚀是金属原子失去电子变成阳离子被氧化的过程,D正确;答案选B。
【题型】单选题
【结束】
23
【题目】下列说法不正确的是
A. 麦芽糖及其水解产物均能发生银镜反应
B. 用溴水即可鉴别苯酚溶液,2,4-已二烯和甲苯
C. 在酸性条件下,![]() 的水解产物是
的水解产物是![]() 和
和![]()
D. 用甘氨酸![]() 和丙氨酸
和丙氨酸![]() 缩合最多可形成4种二肽
缩合最多可形成4种二肽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲配制100mL0.20mol·L-1的KCl溶液,实验操作如下:
A. 用托盘天平准确称取1.49gKCl固体,并放入烧杯中;
B. 加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,并恢复至室温;
C .将KCl溶液由烧杯小心倒入100mL容量瓶中;
D .然后往容量瓶中加蒸馏水,直到液面接近标线1-2cm处,轻轻摇动容量瓶并静置片刻后,改用胶头滴管滴加蒸馏水;
E.使溶液凹面最低点恰好与刻度相切,把容量瓶盖好,上下翻转摇匀后装瓶。
(1)该学生操作中错误的是____________(填写字母序号)。
(2)下面哪些操作会导致所配的100mL0.20mol/L的KCl溶液浓度降低___________。
A 容量瓶用蒸馏水洗涤三次直到洗净 B 称量KCl固体时将砝码放在左盘
C 未洗涤转移KCl溶液的烧杯 D 转移KCl溶液时有KCl溶液溅出
E 定容时仰视刻度线
(3)若用0.2mol·L-1的KCl溶液配制0.05mol·L-1的KCl溶液200.0mL,需要0.20mol·L-1的KCl溶液____________mL。
(4)若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________mol/L。(填字母)
A ![]() B
B ![]() C
C ![]()
![]() D
D ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于燃烧热的描述中正确的是( )
A. 已知a g乙烯气体充分燃烧时生成1 mol CO2和液态水,放出b kJ的热量,则表示乙烯燃烧热的热化学方程式为2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH=-4b kJ·mol-1
B. 将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1
C. H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
D. 葡萄糖的燃烧热是2800kJ·mol-1,则![]() C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) ΔH=-1400kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.0.1mol·L-1NaOH溶液:Na+、K+、![]() 、
、![]()
B.0.1mol·L-1Fe2(SO4)3溶液:Cu2+、![]() 、SCN-、
、SCN-、![]()
C.0.1mol·L-1Na2S溶液:Na+、K+、ClO-、OH-
D.0.1mol·L-1NH4HCO3溶液:Ba2+、K+、OH-、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将氨水与氯化铵溶液混合得到c(NH3·H2O)+c(NH4+)=0.l mol·L-1的溶液。溶液中c(NH3·H2O)、c(NH4+)与pH的关系如下图所示。下列有关离子浓度关系叙述一定正确的是( )
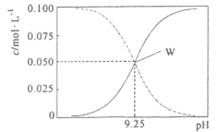
A.W点表示溶液中:c(NH3·H2O)+c(H+)=c(Cl-)+c(OH-)
B.pH=7.0溶液中: c(NH3·H2O)>c(NH4+)>c(OH-)=c(H+)
C.pH=10.5的溶液中:c(Cl-)+c(OH-)+c(NH3·H2O)<0.1 mol·L-1
D.向W点所表示的1 L溶液中加入0.05 mol NaOH固体(忽略溶液体积变化):c(Na+)>c(Cl-)>c(OH-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沼气是重要的生物质能,主要由有机废弃物发酵产生,其成分有CH4、CO2和H2S等,由沼气获得高纯度CH4的工作原理如图所示(交换膜左侧为酸性溶液,右侧为碱性溶液),下列说法中错误的是
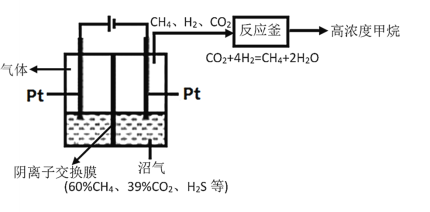
A.对沼气池进行检修时应预先通风并戴防毒面具
B.阴离子应从左侧向右侧迁移
C.在阳极上可能发生反应:HS--2e-=S↓+H+
D.一定条件下反应釜中的反应能自发进行,主要原因是该反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁二酮肟镍是丁二酮肟在氨性溶液(pH=8~9)中与Ni2+发生反应生成的沉淀,该反应常用作实验室中检验镍离子。其结构如图所示,下列对该物质的分析与判断中,正确的是

A.该物质中Ni原子具有空轨道,是配合物的配体
B.该物质中C、N、O原子存在孤电子对
C.该物质的分子中含有的化学键有共价键和配位键
D.该物质中碳原子的杂化类型均为sp2杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com