
【题目】高分子化合物![]() 的合成路线如下:
的合成路线如下:
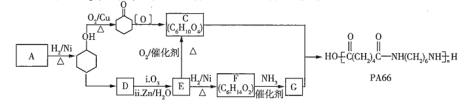
已知: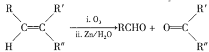 。
。
(1)![]() 的相对分子质量为94,属于芳香化合物,其结构简式是____________。
的相对分子质量为94,属于芳香化合物,其结构简式是____________。
(2)![]() 的反应条件是__________;
的反应条件是__________;![]() 的化学方程式是__________________。
的化学方程式是__________________。
(3)![]() 中所含官能团的名称是_______________。
中所含官能团的名称是_______________。
(4)![]() 有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式:_______________。
有多种同分异构体,写出符合下列条件的一种同分异构体的结构简式:_______________。
i.属于醇类 ii.所有碳原子之间均以单键相连
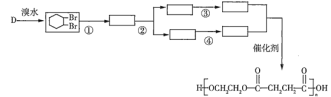
(5)只用有机物![]() 可合成聚丁二酸乙二酯,请结合题中信息补充完整下列合成路线__________(方框中用结构简式表示有机物,用箭头表示转化关系,在箭头上注明试剂和反应条件)。
可合成聚丁二酸乙二酯,请结合题中信息补充完整下列合成路线__________(方框中用结构简式表示有机物,用箭头表示转化关系,在箭头上注明试剂和反应条件)。
【答案】![]() 浓硫酸、加热
浓硫酸、加热 ![]() 羟基
羟基 ![]()

【解析】
由A与H2反应后的生成物环己醇可知,一个A分子中含有一个O原子,因为A的相对分子质量为94,所以A的分子式为C6H6O,又因为A属于芳香化合物,故A的结构简式为![]() ;结合题中的已知信息,要使D转化为E,D中必须含有碳碳双键,故环己醇(
;结合题中的已知信息,要使D转化为E,D中必须含有碳碳双键,故环己醇(![]() )在一定条件下发生消去反应生成D,D的结构简式为
)在一定条件下发生消去反应生成D,D的结构简式为![]() ,E为OHC(CH2)4CHO,结合C的分子式C6H10O4,E发生催化氧化生成C,故C的结构简式为HOOC(CH2)4COOH,结合F的分子式,E与H2发生加成反应生成F,F的结构简式为HOH2C(CH2)4CH2OH,有高分子化合物PA66的结构简式可知,C与G发生缩聚反应生成PA66,故G的结构简式为H2N(CH2)6NH2。
,E为OHC(CH2)4CHO,结合C的分子式C6H10O4,E发生催化氧化生成C,故C的结构简式为HOOC(CH2)4COOH,结合F的分子式,E与H2发生加成反应生成F,F的结构简式为HOH2C(CH2)4CH2OH,有高分子化合物PA66的结构简式可知,C与G发生缩聚反应生成PA66,故G的结构简式为H2N(CH2)6NH2。
(1)由分析可知A的分子式为C6H6O,又因为A属于芳香化合物,故A的结构简式为![]() ;
;
(2)由分析知D为环己烯,故环己醇在浓硫酸、加热的条件下发生消去反应生成环己烯;E→C的化学方程式为![]() ;
;
(3)F的结构简式为HOH2C(CH2)4CH2OH,F所含官能团的名称为羟基;
(4)A的分子式为C6H6O,属于醇类,所有碳原子之间均以单键相连,只能是环状结构,同分异构体的结构简式为![]() ;
;
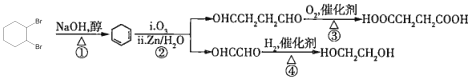
(5)D为环己烯(![]() ),
),![]() 与溴水中的Br2发生加成反应生成
与溴水中的Br2发生加成反应生成![]() ,
,


科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是
A.含28g硅的SiO2晶体中存在的共价键总数为2NA
B.标准状况下,2.24L乙烯中含有的π键数目为0.1NA
C.室温时,pH=2的盐酸中H+数目为1.0×10-2NA
D.124gP4(正四面体)中P-P键数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CF3COOH水溶液中将甲烷直接转化为CF3COOCH3(水解生成CH3OH)的反应机理如图,下列说法正确的是
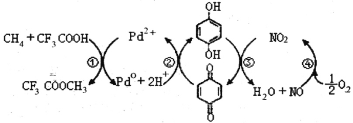
A.所含部分元素第一电离能:C<N<O<F
B.反应③的氧化剂为对苯二酚
C.上述反应的总反应式为:CH4+CF3COOH+![]() O2
O2 CF3COOCH3+H2O
CF3COOCH3+H2O
D.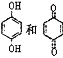 均可以与浓溴水反应,且反应类型相同
均可以与浓溴水反应,且反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
CH3CH2CH2CHO;利用如图装置用正丁醇合成正丁醛相关数据如表:
物质 | 沸点/℃ | 密度 / gcm-3 | 水中溶解性 |
|
正丁醇 | 117.2 | 0.8109 | 微溶 | |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是
A.为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B.当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
C.反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D.向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

(1)仪器a的名称是_______,仪器b的名称是_______。b中利用质量分数为70%80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-Fe(S2O3)33-(紫黑色)
装置 | 试剂X | 实验现象 |
| Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294gmol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作与预期实验目的或所得实验结论一致的是
选项 | 实验操作和现象 | 预期实验目的或结论 |
A | 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色 | 说明该食盐试样不含KIO3 |
B | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
C | 向两支盛有KI3的溶液的试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在平衡: |
D | 室温下向CuCl2和少量FeCl3的混合溶液中,加入铜屑,充分搅拌,过滤,得蓝绿色溶液 | 除去杂质FeCl3得纯净CuCl2溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)(CH3)3 NH+和![]() 可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂___________(填“大”或“小”),可用作___________(填序号)。
可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂___________(填“大”或“小”),可用作___________(填序号)。
a.助燃剂 b.“绿色”溶剂 c.复合材料 d.绝热材料
(2)为了研究在纳米级的空间中水的结冰温度,科学家对不同直径碳纳米管中水的结冰温度进行分析。如图是四种不同直径碳纳米管中的冰柱结构及结冰温度,冰柱的大小取决于碳纳米管的直径。水在碳纳米管中结冰的规律是_________________。
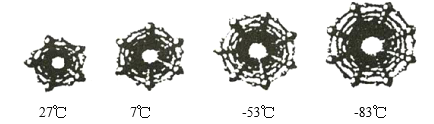
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向淀粉-碘化钾的酸性溶液中加入少量 H2O2 溶液,溶液立即变蓝,再向蓝色溶液中缓慢通入足量的 SO2, 蓝色逐渐消失。下列判断不正确的是
A.根据上述实验判断 H2O2 和 SO2 反应能生成强酸
B.蓝色逐渐消失,体现了 SO2 的漂白性
C.SO2 中 S 原子采取 sp2杂化方式,分子的空间构型为 V 型
D.H2O2是一种含有极性键和非极性键的极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋(Bi)及其化合物广泛应用于电子、医药等领域。一种以含铋矿石辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)为原料,采用湿法冶金制备铋单质的工艺流程如下:
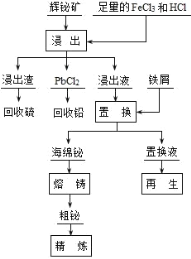
已知:PbCl2是一种难溶于冷水,易溶于热水的白色固体。 回答下列问题:
(1)铋(Bi)位于ⅤA族,铋的氢化物的热稳定性______氨气(填“大于”或“小于”)。
(2)“浸出”时,为了提高浸出速率,可采用的措施有______(任写一条)
(3)加热浸出时,PbO2 生成 PbCl2 和一种气体,此反应的化学方程式为______, 从产物中分离回收 PbCl2 的步骤是______、洗涤、干燥。从保护环境和原料循环利 用的角度,请指出上述工艺流程中可以采取的措施为______。
(4)电解精炼粗铋时必须补充含 Bi3+浓度高的电解液。可用粗铋、铅条作为两个电极,铅条外用素烧 的陶瓷坩埚作隔膜(Bi3+不能透过,H+能透过),电解液开始时为盐酸和食盐的混合液。则粗铋为电解池的 ______极,电解总反应为______。
(5)25℃时,向浓度均为 0.02mol·L-1 的 Cu2+、Bi3+的混合溶液中滴加 Na2S 溶液(设溶液体积增加 1倍),使 Cu2+恰好沉淀完全即溶液中 c(Cu2+)=1×10-5 mol·L-1,此时是否有 Bi2S3 沉淀生成______(列式计算说明)。(已知:25℃时,Ksp(CuS)=6.0×10-36、Ksp(Bi2S3)=1.8×10-99)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com