
| A、A0.7L | B、1.4L |
| C、1.6L | D、2.8L |
| y |
| 4 |
| y |
| 2 |
| y |
| 4 |
| y |
| 2 |
| xmol×1+ymol×2 |
| xmol+ymol |
| 2 |
| 2+3 |
| 2 |
| 2+3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Fe3+、Ba2+、K+、HCO-3、SCN-、Cl- |
| B、Mg2+、Na+、K+、SO42-、Br-、HSO-3 |
| C、Ba2+、Al3+、K+、Cl-、HCO-3、NO-3 |
| D、Fe3+、Na+、NH4+、SO42-、NO-3、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、用图1作为气体发生装置,液体由分液漏斗加入与烧瓶中固体反应,产生的难溶于水的气体用排水法测量气体体积时,排出的水的体积扣除分液漏斗加入的液体体积即为产生气体的体积 |
| B、用图2测量难溶于水的气体体积时,如果气体滞留在烧瓶中,会导致测定的氢气体积偏小 |
| C、用图3可以完成喷泉实验 |
| D、图4可以“随开随用,随关随停”地用于一些气体的制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl溶液焰色反应呈黄色 |
| B、NH3能使湿润的红色石蕊试纸变蓝 |
| C、漂白粉的主要成分是次氯酸钙和氯化钙 |
| D、进行蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
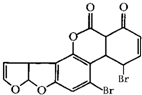 某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )
某有机物是一种强致癌物,其结构如图所示.1mol该化合物在一定条件下分别与H2、NaOH溶液反应,最多消耗H2和NaOH的物质的量分别为( )| A、6mol、4mol |
| B、7mol、4mol |
| C、7mol、5mol |
| D、6mol、5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150 mL 1 mol?L-1氯化钠溶液 |
| B、75 mL 1.5 mol?L-1氯化钙溶液 |
| C、150 mL 3 mol?L-1氯化钾溶液 |
| D、50 mL 3 mol?L-1氯化镁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
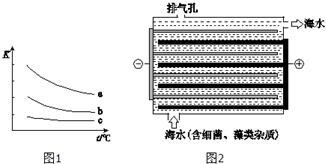 海水是巨大的化学资源宝库.
海水是巨大的化学资源宝库.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com