
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是

A. 相对于途径①,途径②更好地体现了绿色化学思想
B. Y可以是葡萄糖溶液
C. 利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1 mol
D. 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2
【答案】C
【解析】试题分析:A.相对于途径①、③,途径②的优点:制取等质量胆矾需要的硫酸少、途径2无污染性气体产生,故A正确;B.葡萄糖与氢氧化铜反应的方程式为:C6H12O6+2Cu(OH)2=C6H12O7+Cu2O+2H2O,所以Y可为葡萄糖,故B正确;C.在途径②中氧化剂是氧气,铜是还原剂,硫酸不是氧化剂也不是还原剂,故C错误;D.Cu与混酸反应,3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,离子反应为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,从方程式知,硝酸根离子由硝酸提供,氢离子由硝酸和硫酸提供,所以硝酸为2mol时,硫酸为3mol,混酸中H2SO4与HNO3物质的量之比最好为3:2,故D正确;故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1)常温下,如果取0.1molL-1HA溶液与0.1molL-1NaOH溶液等体积混合(混合后溶液体积的变化忽略不计),测得混合液的pH=8。
①混合液中由水电离出的OH-浓度与0.1molL-1NaOH溶液中由水电离出的OH-浓度之比为_________;
②已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH _____7(填“<”、“>”或“=”);相同温度下,等物质的量浓度的下列四种盐溶液按pH由大到小的排 列顺序为_________(填序号)。
a.NH4HCO3 b.NH4A c.(NH4)2CO3 d.NH4Cl.
(2)清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。
一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)CH3OH(g)△H=-105kJmol-1.向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是_________;
②反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=_________;
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=_________;
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____T3(填“>”“<”“=”),判断的理由是_________;
(3)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e=2O2-)

①c电极为_________正极,d电极上的电极反应式为_________;
②图乙是用惰性电极电解100mL 0.5molL-1 CuSO4溶液,a电极上的电极反应式为_________;若a电极产生56mL(标准状况)气体,则所得溶液的pH=_________(不考虑溶液体积变化),若要使电解质溶液 恢复到电解前的状态,可加入_________(选填字母序号)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
(3)若该物质能和钠反应产生氢气,试写出该物质的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊二烯(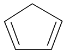 )是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
)是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
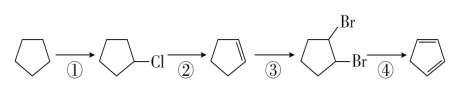
(1)其中,反应①的反应类型是______ ______,反应①的产物名称是____ ____;
反应②的反应类型是____ ____,反应②的产物名称是___ _____。
工业上可由环戊二烯制备金刚烷( ),途径如下:
),途径如下:

请回答下列问题:
(2)环戊二烯分子中最多有________个原子共平面;
(3)金刚烷的分子式为________,其分子中的二氯代物有________种;
(4)A是二聚环戊二烯的同分异构体,属于芳香烃,其苯环上的一氯代物只有二种,能使溴的四氯化碳溶液褪色。符合以上信息的A的所有可能结构(不考虑立体异构)有 种,试写出苯环上支链最多的几种同分异构体的结构简式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效,苹果醋是一种常见的有机酸,其结构简式为

(1)苹果醋中含有的官能团的名称是________________。
(2)苹果醋的分子式为________。
(3)1 mol苹果醋与足量Na反应,能生成标准状况下的H 2 ________L。
(4)苹果醋可能发生的反应是________。
A.与NaOH溶液反应
B.与石蕊试液作用
C.与乙酸在一定条件下发生酯化反应
D.与乙醇在一定条件下发生酯化反应
(5)两分子苹果醋发生酯化反应成C8H10O9的链状酯有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的以离子形式存在的碘元素。下图是实验室从海藻中提取碘的流程的一部分。
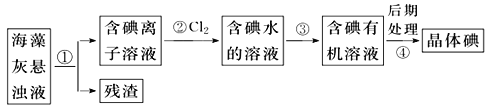
下列判断正确的是( )
A. 步骤①、③的操作分别是过滤、萃取
B. 可用硝酸银溶液检验步骤②的反应是否进行完全
C. 步骤③中加入的有机溶剂是裂化汽油或四氯化碳
D. 步骤④的操作是过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的下列有机物,充分燃烧,消耗氧气的量相同的是
A. C3H4和C2H6
B. C3H6和C3H8O
C. C3H6O2和C3H8O
D. C3H8O和C4H8O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用一种试剂可以区别MgCl2、FeCl2、AlCl3三种溶液,这种试剂是( )
A.AgNO3溶液 B.NAOH溶液 C.硫酸 D.KNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(本题满分18分)钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:

已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解.
请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有 ,操作2是 、过滤,副产品主要成分的化学式为 。
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理 。
(3)已知钛的还原性介于铝和锌之间,估计钛能耐腐蚀的原因之一是,如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式为 。
(5)为测定溶液中TiOSO4的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3TiO2++Al+6H+═3Ti3++AlO3++3H2O,过过滤后,取出滤液20.00mL,向其中滴加2~3滴KSCN溶液作指示剂,用 (填一种玻璃仪器的名称)滴加0.1000molL﹣1FeCl3溶液,发生Ti3++Fe3+═Ti4++Fe2+,当溶液出现红色达到滴定终点,用去了30.00mLFeCl3溶液,待测钛液中TiOSO4的物质的量浓度是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com