
����Ŀ���������ֶ�����Ԫ�آ�H ��C ��N ��O ��Na ��Cl��
��1��������γɵĻ�����ĵ���ʽ��__________����ҵ�����øû������Ʊ�NO�Ļ�ѧ����ʽ___________��
��2���ݵĵ����ڢܵĵ�����ȼ�գ����ɵ���ɫ���塣�ò���ĵ���ʽ��______________________________���ò����к��еĻ�ѧ����������______________________________��
��3���ں͢���̬�⻯�������ȶ��Խ�ǿ����__________���û�ѧʽ��ʾ�����ܱ�ʾ���ں͢����������ˮ���������ǿ���Ļ�ѧ����ʽ��______________________________��
���𰸡� ![]() 4NH3+5O2
4NH3+5O2![]() 2N2+6H2O
2N2+6H2O ![]() �Ǽ��Թ��ۼ������Ӽ� HCl Na2CO3+2HClO4=2NaClO4+H2O+CO2��
�Ǽ��Թ��ۼ������Ӽ� HCl Na2CO3+2HClO4=2NaClO4+H2O+CO2��
�������� (1)H��N�γɵĻ�����NH3Ϊ���ۻ���������ʽ��![]() ������NH3�Ļ�ԭ�ԣ�ͨ�����Ĵ������ɵõ�NO��������Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2
������NH3�Ļ�ԭ�ԣ�ͨ�����Ĵ������ɵõ�NO��������Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2![]() 2N2+6H2O��
2N2+6H2O��
(2)Na��������ȼ�գ����ɵ���ɫ����Na2O2�������ӻ�����ĵ���ʽ��![]() �����еĻ�ѧ���������ǷǼ��Թ��ۼ������Ӽ���
�����еĻ�ѧ���������ǷǼ��Թ��ۼ������Ӽ���
(3)Cl�ķǽ����Ա�Cǿ����HCl���ȶ��Ա�CH4ǿ������ǿ���������ԭ��������HClO4�����Ա�̼��ǿ�Ļ�ѧ����ʽ�� Na2CO3+2HClO4=2NaClO4+H2O+CO2����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨij�л�������A�Ľṹ����������ʵ�飺
(1)���л���A�����������г��ȼ�գ�ʵ���ã�����5.4 g H2O��8.8 g CO2����������6.72 L(��״����)�����������ʵ��ʽ��________��
(2)�������Dzⶨ���л����������Է����������õ���ͼ����ʾ����ͼ��������Է�������Ϊ__________�������ʵķ���ʽ��________��
(3)�˴Ź��������ܶ��л�������в�ͬ��ѧ��������ԭ�Ӹ�����ͬ�ķ�ֵ(�ź�)�����ݷ�ֵ(�ź�)����ȷ����������ԭ�ӵ��������Ŀ�����磺���ȼ���(ClCH2OCH3)��������ԭ����ͼ�ڡ����ⶨ���л���A�ĺ˴Ź�������ʾ��ͼ��ͼ�ۣ���A�Ľṹ��ʽΪ__________��



�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ͬ���칹�����
���Զ��ױ����ұ������Ҵ����Ҷ�������1�ȱ����2�ȱ��飻����ϩ�ͻ����飻����ϩ�;���ϩ
A. �٢ڢۢܢ�B. �٢ۢ�C. �ڢۢ�D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ƕ�ʮ���;�ʮ�����չ������һ��������ɫ��أ����и�������������������Ⱦ���ص㡣������������������̼�ܵȲ��������Ķ��ε�ص�ԭ����ͼ��ʾ����ص��ܷ�ӦʽΪ��


����ͼ�� ����ͼ��
��1���������س��ʱ�����缫����ֱ����Դ��___________���������ĵ缫��ӦʽΪ____________��
�������طŵ�ʱ��OH������____________���̼�缫�������缫������
��2������������̼�ܵȲ��ϴ����⣬����ʹ���л�������û�����ͱ�֮��Ŀ��淴Ӧ��ʵ������ͼ��⡣һ�������£�������ͼװ�ÿ�ʵ���л���ĵ绯ѧ���⣨���������л����
��AΪ��Դ��____________����
�ڵ缫E�ϲ���������Ϊ____________��
�۵缫D�ĵ缫��ӦʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����������������ԭNO3-�ѳ�����ˮ�������Ρ���������Ϻ���������װ��̽��������KNO3��Һ�ķ�Ӧ��ʵ�鲽�輰�������£�
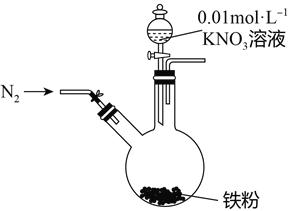
ʵ�鲽�� | ʵ������ |
1�����ɼУ�����ͨ��N2 | |
2������pHΪ2.5��0.01mol/L����KNO3��Һ100mL | ���۲����ܽ⣬��Һ��dz��ɫ�� ���۲����ܽ��ʣ�����۱������������ɫ���ʸ��š� |
3����Ӧֹͣ�ε���������Բ����ƿȡ�� | ��ƿ���������ɫû�з����仯�� |
4����ʣ�������� | ����İ�ɫ���ʱ�Ϊ���ɫ�� |
��1��ͨ��N2�����ֺ�����Ӧ����N2��Χ�н��е�ʵ��Ŀ����______________________________��
��2����ɫ������__________���û�ѧ����ʽ�������Ϊ���ɫ��ԭ��____________________��
��3��Ϊ��̽���Һ�ijɷ֣���ͬѧ��һ�����������ʵ�飺
ʵ�鲽�� | ʵ������ |
1��ȡ������Һ���Թ��У������м���KSCN��Һ | ��ҺҺ�ޱ仯 |
2����������Һ��Ϊ���ݣ�һ���е�����������һ���еμ�ϡ���� | ������Һ����Ϊ��ɫ |
3����ȡ������Һ���Թ��У������м���ŨNaOH��Һ�����ȣ����Թܿڷ���ʪ��ĺ�ɫʯ����ֽ�� | ���������ɣ�������ʹ��ɫʯ����ֽ������ |
��i����������ʵ���������ж���Һ�д���____________________���ӡ�
��ii������2�еμ�ϡ�������Һ����dz��ɫ��ɺ�ɫ���������ӷ���ʽ������ԭ��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������л����˵������ȷ���� �� ��
A. ����������鶼���� B. ���ͼ������ʹ����KMnO4��Һ��ɫ
C. �������ϩ��������������Ӧ D. ��ϩ���������������ӳɷ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��Ba(OH)2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ�����з�������ȷ����( )
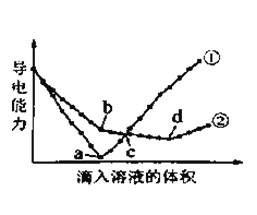
A. �������μ�H2SO4��Һ�ı仯����
B. b�㣬��Һ�д������ڵ�������Na+��OH�C
C. c�㣬����Һ�к�����ͬ����OH�C
D. a��d�����Ӧ����Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����¯�����Ļ�����Ӧ֮һ�ǣ�FeO(s)+CO(g) ![]() Fe(s)+CO2(g) ����H>0����ƽ �ⳣ��K=
Fe(s)+CO2(g) ����H>0����ƽ �ⳣ��K=![]() ����K(1100��)=0.263��
����K(1100��)=0.263��
(1) �¶����ߣ�ƽ�ⳣ��K��ֵ______����¯��CO2��CO�������ֵ______���� ��������������С��������������
(2)��1100��ʱ�����ij��¯�У�c(CO2)=0.025mol/L��c(CO)=0.1mol/L�������� ���£��÷�Ӧ�Ƿ���ƽ��״̬����_____����ǡ�����������ʱ����ѧ��Ӧ������V(��)__________V(��)(����ڡ��������ڡ�����С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL0.1mol/L��MOH��Һ��μ���һ��Ũ�ȵ�HA��Һ�μӹ�����,��Һ��pH�����HA��Һ�������ϵ��ͼ��ʾ����pH=8ʱMOH��Һǡ�ñ��к͡�������˵���������
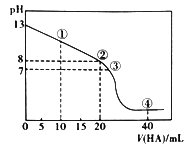
A. �ڵ�����Һ��ˮ�������c(H+)����HA��Һ����ˮ�������c(H+)
B. �۵�����Һ�и�����Ũ�ȵĴ�С��ϵ��c(M+)=c(A-)>c(H+)=c(OH-)
C. ��HA��Һ��Ũ��Ϊ0.1mol/L
D. ������Һ��������c(HA)+c(H+)>c(M+)+c(OH-)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com