
| A.有机物不导电 | B.金刚石是自然界最硬的物质 |
| C.SO2可用作食品防腐剂 | D.NO可用于某些疾病的治疗 |
科目:高中化学 来源:不详 题型:单选题
| A.H2S | B.S | C.FeS | D.FeSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2对环境的主要影响是形成酸雨 |
| B.用天然气、水煤气等清洁燃料代替煤炭作民用燃料或在煤中加入生石灰后燃烧,可以减少SO2的排放量 |
| C.硫酸厂使用V2O5作催化剂,加快SO2的转化速率,可以减少SO2的排放量 |
| D.植树造林,绿化环境有利于减少空气中SO2的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
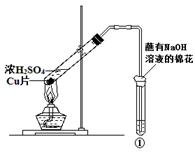
| | ①中试剂 | ①中现象 | 解 释 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验操作 | 预期现象 | 结 论 |
| 验证猜想Ⅰ | 步骤①:取少量0.01 mol/L 酸性KMnO4溶液,滴入所得溶液中 | | |
| 步骤②: | | 含有Fe3+ | |
| 验证猜想Ⅱ | 将所得气体通入如下装置 | | 含有两种或以上气体 |
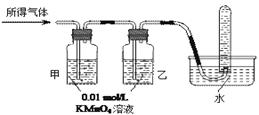
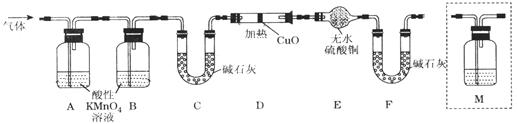
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
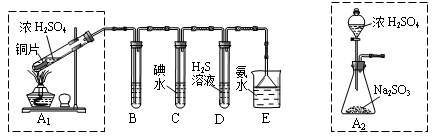
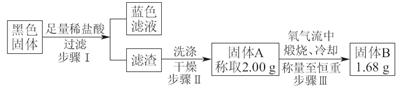
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe2(SO4)3+SO2↑+6H2O)。
Fe2(SO4)3+SO2↑+6H2O)。| A.小于20. 16 L | B.等于20. 16 L |
| C.介于20. 16 L和40. 32 L之间 | D.等于40. 32 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com