
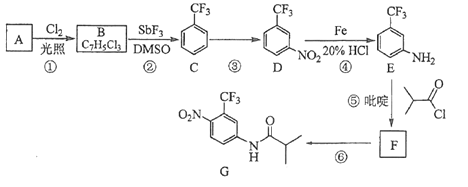
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
回答下列问题:
(1)G的分子式是________。
(2)③的反应试剂和反应条件分别是________________,该反应的类型是________。
(3)⑤的反应方程式为________,吡啶是一种有机碱,其作用是________。
(4)G中所含官能团的名称为________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有________种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )与乙酰氯(
)与乙酰氯(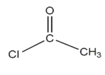 )制备4-甲氧基乙酰苯胺的合成路线(其他无机试剂任选);________________
)制备4-甲氧基乙酰苯胺的合成路线(其他无机试剂任选);________________
【答案】C11H11N2F3O3 浓硫酸、浓硫酸,加热 硝化反应(或取代反应) 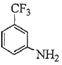 +
+![]()
![]() HCl+
HCl+ 吸收反应产物的HCl,提高反应转化率 硝基、氟原子、肽键 9种
吸收反应产物的HCl,提高反应转化率 硝基、氟原子、肽键 9种 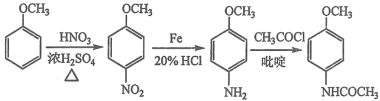
【解析】
由B的分子式可知A为甲苯,则B为三氯甲苯,C为三氟甲苯,发生硝化反应生成D,D还原生成E,E与![]() 发生取代反应生成F为
发生取代反应生成F为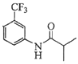 ,然后发生硝化反应生成G,结合对应的有机物的结构和性质解答。
,然后发生硝化反应生成G,结合对应的有机物的结构和性质解答。
(1)根据G的结构简式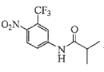 可知,其分子式为C11H11N2F3O3;
可知,其分子式为C11H11N2F3O3;
(2)③的反应是![]() 在浓硫酸催化下与浓硝酸在加热条件下发生硝化反应(或取代反应)生成
在浓硫酸催化下与浓硝酸在加热条件下发生硝化反应(或取代反应)生成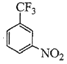 和水,试剂和反应条件分别是浓硫酸、浓硫酸,加热;该反应的类型是硝化反应(或取代反应);
和水,试剂和反应条件分别是浓硫酸、浓硫酸,加热;该反应的类型是硝化反应(或取代反应);
(3)⑤的反应是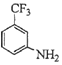 与
与![]() 在吡啶作用下发生取代反应生成
在吡啶作用下发生取代反应生成 和氯化氢,反应的化学方程式为
和氯化氢,反应的化学方程式为 +
+![]()
![]() HCl+
HCl+ ,吡啶是一种有机碱,吡啶的作用是吸收反应产物的HCl,提高反应转化率;
,吡啶是一种有机碱,吡啶的作用是吸收反应产物的HCl,提高反应转化率;
(4)G为 ,所含官能团的名称为硝基、氟原子、肽键;
,所含官能团的名称为硝基、氟原子、肽键;
(5)-CF3和-NO2处于邻位,另一个取代基在苯环上有3种位置,-CF3和-NO2处于间位,另一取代基在苯环上有4种位置,-CF3和-NO2处于对位,另一个取代基在苯环上有2种位置,因此共有9种结构。
(6)根据目标产物和流程图,苯甲醚应首先与混酸反应,在对位上引入硝基,然后在铁和HCl作用下-NO2转化成-NH2,最后在吡啶作用下与CH3COCl反应生成目标产物,合成路线是: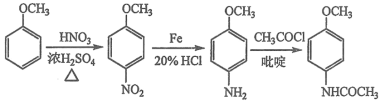 。
。


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,体积为2L的密闭容器中,1molX和3molY进行反应:X(g)+3Y(g)![]() 2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是( )
2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是( )
A.以X浓度变化表示的反应速率为1/8mol/(L·S)
B.12s后将容器体积扩大为10L,Z的平衡浓度变为原来的1/5
C.若增大X的浓度,则物质Y的转化率减小
D.若该反应的△H<0 ,升高温度,平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质易溶于水的是________,易溶于CCl4的是________。(均填编号)
①NH3 ②CH4 ③![]() ④HCl ⑤C2H4 ⑥Br2 ⑦HNO3 ⑧H2S
④HCl ⑤C2H4 ⑥Br2 ⑦HNO3 ⑧H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:2SO3(g) ![]() 2SO2(g)+O2(g)、2NO(g)+O2(g)
2SO2(g)+O2(g)、2NO(g)+O2(g) ![]() 2NO2(g) (不考虑NO2和N2O4之间的相互转化),当加入一定量的SO3使上述系统达到平衡时,n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO2气体的物质的量为( )
2NO2(g) (不考虑NO2和N2O4之间的相互转化),当加入一定量的SO3使上述系统达到平衡时,n(O2)=0.1 mol、n(NO2)=3.6 mol,则此时SO2气体的物质的量为( )
A.0.1 molB.3.6 molC.1.8 molD.3.8 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: ①C6H12O6(s)=2C2H5OH(l)+2CO2(g) △H1
②6CO2(g)+6H2O(g)=C6H12O6(s)+6O2 △H2
③2H2O(g)=2H2(g)+O2(g) △H3
④2CO2(g)+6H2(g)=C2H5OH(l)+3H2O △H4
下列有关说法正确的是
A. H2的燃烧热为![]()
B. 反应①使用催化剂,△H1将减小
C. 标准状况下,反应②生成1.12LO2,转移的电子数为0.1×6.02×1023
D. 2△H4=△H1+△H2-6△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种无色无味的气体,微溶于水,易溶于有机溶剂。实验室常用如图所示装置制取乙炔,并验证乙炔的性质。完成实验,观察实验现象,回答下列问题:

(1)写出电石(碳化钙CaC2)与水反应,制取乙炔的化学方程式_________________
(2)用饱和食盐水代替蒸馏水的目的是__________________
(3)装置A的作用是_______________,装置B中的现象是__________________
(4)如果要进行乙炔的可燃性实验,首先应该__________________。
(5)若乙炔加氢后得到乙烷,则乙烷在光照条件下与氯气反应,生成的一氯代烷最多有__________种。
(6)若称取a g CaC2,反应完全后,将生成的乙炔全部通入足量溴的CCl4溶液中溶液增重b g,则CaC2的纯度为___________(用百分数表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年度国家科学技术奖授予我国诺贝尔奖获得者屠呦呦,表彰她在抗疟疾青蒿素方面的研究。
(查阅资料)青蒿素熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水几乎不溶。
I.实验室用乙醚提取青蒿素的工艺流程如下:

(1)在操作I前要对青蒿进行粉碎,其目的是________________
(2)操作II的名称是_____________。
(3)操作III进行的是重结晶,其操作步骤为_____ 、_____、______、过滤、洗涤、干燥
II.已知青蒿素是一种烃的含氧衍生物为确定它的化学式,进行了如下实验:

实验步骤:①连接装置,检查装置的气密性。②称量E、F中仪器及药品的质量。③取14.10g青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量。
(4)装置E、F应分别装入的药品为_______________、___________________。
(5)实验测得:
装置 | 实验前 | 实验后 |
E | 24.00g | 33.90g |
F | 100.00g | 133.00g |
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为______。
(6)若使用上述方法会产生较大实验误差,你的改进方法是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室使用pH传感器来测定![]() 和
和![]() 混合物中
混合物中![]() 的含量,称取
的含量,称取![]() 样品,溶于水配成
样品,溶于水配成![]() 溶液,取出该溶液
溶液,取出该溶液![]() 用
用![]() 盐酸滴定,得到图曲线.下列说法不正确的是
盐酸滴定,得到图曲线.下列说法不正确的是![]()

A.此样品![]()
B.计量点![]() 溶液中大量存在的阴离子是
溶液中大量存在的阴离子是![]()
C.计量点![]() 之间发生反应的离子方程式为
之间发生反应的离子方程式为![]()
D.使用该方法测定![]() 和NaOH混合溶液中的NaOH含量,将会得到1个计量点
和NaOH混合溶液中的NaOH含量,将会得到1个计量点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com