
【题目】实验室使用pH传感器来测定![]() 和
和![]() 混合物中
混合物中![]() 的含量,称取
的含量,称取![]() 样品,溶于水配成
样品,溶于水配成![]() 溶液,取出该溶液
溶液,取出该溶液![]() 用
用![]() 盐酸滴定,得到图曲线.下列说法不正确的是
盐酸滴定,得到图曲线.下列说法不正确的是![]()

A.此样品![]()
B.计量点![]() 溶液中大量存在的阴离子是
溶液中大量存在的阴离子是![]()
C.计量点![]() 之间发生反应的离子方程式为
之间发生反应的离子方程式为![]()
D.使用该方法测定![]() 和NaOH混合溶液中的NaOH含量,将会得到1个计量点
和NaOH混合溶液中的NaOH含量,将会得到1个计量点
【答案】D
【解析】
向NaHCO3和Na2CO3混合溶液中滴加稀盐酸时,发生反应的先后顺序是:CO32—+H+=HCO3—, HCO3—+H+=H2O+CO2↑,两个计量点①和②,0~11.9mL时发生CO32—+H+=HCO3—,①是CO32—恰好完全转化成HCO3—的点,11.9~28.1mL发生HCO3—+H+=H2O+CO2↑,②是HCO3—完全转化成CO2的点。
A.根据图知,0~11.9mL时发生的反应为CO32—+H+=HCO3—、11.9~28.1mL时发生的反应为HCO3—+H+= H2O +CO2↑,11.9~28.1mL发生反应的NaHCO3包含原来的和Na2CO3转化的,原样品中的NaHCO3所消耗的HCl是(28.1—11.9—11.9)mL,根据HCO3—+H+=H2O+CO2↑知,原样品n(NaHCO3)=n(HCl)=(28.1—11.9—11.9)×10—3L×0.01mol/L×10=(28.1—2×11.9)×10—4mol,故A正确;
B.pH=4,溶液显酸性,溶液中溶质为NaCl、H2CO3,则计量点②溶液中大量存在的阴离子是Cl—,故B正确;
C.计量点①~②之间是NaHCO3和稀盐酸的反应,离子方程式为HCO3—+H+= H2O +CO2↑,故C正确;
D.Na2CO3和NaOH混合溶液中滴加稀盐酸,反应先后顺序依次是NaOH、Na2CO3、NaHCO3,所以应该有3个计量点,故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
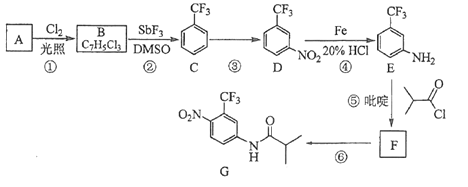
回答下列问题:
(1)G的分子式是________。
(2)③的反应试剂和反应条件分别是________________,该反应的类型是________。
(3)⑤的反应方程式为________,吡啶是一种有机碱,其作用是________。
(4)G中所含官能团的名称为________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有________种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )与乙酰氯(
)与乙酰氯(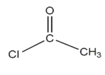 )制备4-甲氧基乙酰苯胺的合成路线(其他无机试剂任选);________________
)制备4-甲氧基乙酰苯胺的合成路线(其他无机试剂任选);________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H22NH3。已知加入1molN2和4molH2时,达到平衡后生成amolNH3.有恒温恒压下欲保持平衡时各组分的体积分数不变.填表(恒温恒压)
已知 编号 | 起始状态物质的量/mol | 平衡时NH3的 物质的量/mol | ||
N2 | H2 | NH3 | ||
1 | 4 | 0 | a | |
① | 1.5 | 9 | 0 | ________ |
② | ________ | ________ | 1 | 0.5a |
③ | m | g(g=4m) | 0 | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) ![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. X的分解速率与Y的消耗速率相等 D. 单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:

A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NiSO4![]() 6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
6H2O易溶于水,其溶解度随温度升高明显增大。以电镀废渣(主要成分是NiO,还有CuO、FeO等少量杂质)为原料制备该晶体的流程如下,下列说法错误的是
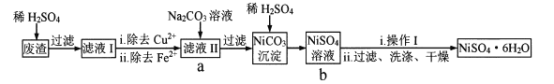
A. 溶解废渣时不能用稀盐酸代替稀H2SO4B. 除去Cu2+可采用FeS
C. 流程中a-b的目的是富集NiSO4D. “操作I”为蒸发浓缩、冷却结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298 K、1.01×105 Pa,将22 g CO2通入0.75 L 1.0 mol·L-1NaOH溶液中充分反应,测得反应放出的热量为a kJ。已知该条件下1 mol CO2通入1 L 2.0 mol·L-1NaOH溶液中充分反应放出的热量为b kJ。则CO2与NaOH反应生成NaHCO3的热化学方程式为( )。
A. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
B. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
C. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
D. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,已知下列三种金属硫化物的溶度积常数(Ksp)分别为:Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=1.3×10-36 ;Ksp(ZnS)=1.6×10-24 。下列关于常温时的有关叙述正确的是( )
A. 硫化锌、硫化铜、硫化亚铁的溶解度依次增大
B. 将足量的ZnSO4晶体加入到0.1 mol·L-1的Na2S溶液中,Zn2+的浓度最大只能达到1.6×10-23 mol·L-1
C. 除去工业废水中含有的Cu2+,可采用FeS固体作为沉淀剂
D. 向饱和的FeS溶液中加入FeSO4溶液后,混合液中c(Fe2+)、Ksp(FeS)都变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体(FeSO4·7H2O)的工艺流程如下:
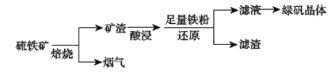
(1)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式________。
(2)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
(3)滤液中金属阳离子的检验方法__________。
(4)FeSO4溶液制备绿矾晶体过程中要保持H2SO4过量,理由________。(结合化学用语说明原因)
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:
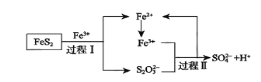
已知总反应为:FeS2+14Fe3++8H2O=2SO42-+15Fe2++16H+
①将过程I离子方程式补充完整______FeS2+______Fe3++_______ ______=7Fe2++______S2O32-+____ ______
②过程II反应的离子方程式________________________________________。
(6)绿矾晶体在空气中易被氧化。取X g样品,加水完全溶解,用酸化的amol·L-1K2Cr2O7溶液滴定至终点,消耗K2Cr2O7溶液b mL。反应原理:6Fe2++Cr2O72-+14H+ =6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为______________。(FeSO4·7H2O摩尔质量为278 g/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com