
【题目】环戊二烯可用于制备二茂铁[Fe(C5H5)2,结构简式为![]() ],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法正确的是( )
],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法正确的是( )
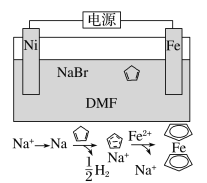
A.该电池工作是,镍连接的是电源的正极
B.可将该电池的DMF惰性有机溶剂更换为NaOH溶液
C.该反应的总反应方程式为Fe+2![]() +H2↑
+H2↑
D.溶液中的Na+离子不断的向Fe附近移动
【答案】C
【解析】
由制备流程可知,Fe失去电子生成Fe2+,Na+得到电子生成Na,所以阳极为Fe电极,Na是中间产物,不参与反应,反应物为Fe和C5H6,生成物为H2和Fe(C5H5)2,因此反应方程式为:Fe+2C5H6= Fe(C5H5)2+ H2↑。
A. Fe失去电子生成Fe2+,阳极为Fe电极,Fe电极与电源的正极相连,A错误;
B. 水会阻碍中间产物Na的生成,且OH-会与Fe2+反应生成Fe(OH)2,所以DMF惰性有机溶剂不能更换为NaOH溶液,B错误;
C. Na是中间产物,不参与反应,反应物为Fe和C5H6,生成物为H2和Fe(C5H5)2,因此反应方程式为:Fe+2![]() +H2↑,C正确;
+H2↑,C正确;
D. 电解池中阳离子移向阴极,阴离子移向阳极,溶液中的Na+离子不断的向Ni附近移动,D错误;
故答案为:C。


科目:高中化学 来源: 题型:
【题目】请阅读下列材料,回答下列小题
将一定比例的三氧化硫和水混合可制得硫酸。硫酸是一种重要的化工原料,用途十分广泛,除用于化学工业外,还非常广泛应用于肥料、非碱性清洁剂、护肤品、油漆添加剂与炸药的制造等方面。
【1】关于浓硫酸的说法正确的是
A.易挥发
B.见光分解
C.密度比水的小
D.常温下能使铝片钝化,浓硫酸作氧化剂
【2】稀硫酸可以用于实验室制氢气,反应方程式为Zn+H2SO4=ZnSO4+H2↑,该反应的反应类型说法正确的是
A.化合反应B.复分解反应C.置换反应D.分解反应
【3】在其他条件不变的情况下,欲提高硫酸与锌反应产生氢气的速率,可以采用的措施有
A.选用颗粒更大的锌粒
B.升高反应温度
C.用98%浓硫酸来代替稀硫酸反应
D.加入硫酸钾溶液
【4】下列反应中,生成物总能量高于反应物总能量的是
A.S+O2![]() SO2
SO2
B.CaO+H2O=Ca(OH)2
C.C+CO2![]() 2CO
2CO
D.Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。某高能锂离子电池的反应方程式为Li1-xCoO2+LixC6![]() LiCoO2+C6(x<l)。以该锂离子电池为电源、苯乙酮为原料制备苯甲酸,工作原理如图所示(注明:酸化电解后的苯甲酸盐可以析出苯甲酸)。
LiCoO2+C6(x<l)。以该锂离子电池为电源、苯乙酮为原料制备苯甲酸,工作原理如图所示(注明:酸化电解后的苯甲酸盐可以析出苯甲酸)。
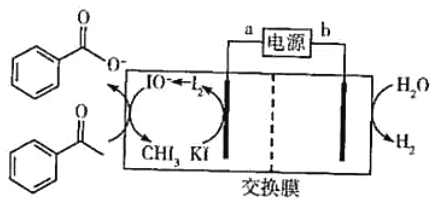
下列说法正确的是( )
A.锂离子电池的a极为负极
B.放电时,正极反应式为xLi++xe-+Li1-xCoO2=LiCoO2
C.交换膜为质子交换膜
D.每产生4.48LH2(标准状况),生成0.4molIO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期的 Cr、Fe、Co、Ni、Cu、Zn 等许多金属能形成配合物。
(1)NH3 是一种很好的配体,氨气分子是_____(填“极性”或“非极性”)分子,NH3 的沸 点_____(填“高于”“等于”或“低于”)AsH3。
(2)科学家通过 X 射线测得胆矾的结构示意图可简单表示如下:

图中虚线表示的作用力为_________________________。
(3)胆矾溶液与氨水在一定条件下可以生成 Cu(NH3)4SO4H2O 晶体。在 Cu(NH3)4SO4·H2O 晶体中,含 有的原子团或分子有:[Cu(NH3)4]2+、NH3、 SO42 、H2O,[Cu(NH3)4]2+为平面正方形结构,则 VSEPR 模型为四面体结构的原子团或分子是_____________,其中心原子的杂化轨道类型是________________ 。
(4)金属镍粉在 CO 气流中轻微加热,生成无色挥发性液态 Ni(CO)4,呈正四面体构型。Ni(CO)4 易溶于_____________________ (填编号)。
a . 水 b. 四氯化碳 c. 苯 d. 硫酸镍溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实与原因对应关系不正确的是
A | B | C | D | |
物质 |
Na2FeO4 |
海水稻 |
金属铜 |
碳酸钠 |
事实 | 用于自来水净水消毒 | 海水稻的秸杆可以燃烧发电 | Cu作原电池的电极 | 制革工业中原料皮的脱脂 |
主要原因 | Na2FeO4有强氧化性且能在水中产生胶体 | 稻子的秸杆中蕴含生物质能 | Cu能导电且质稳定 | Na2CO3稳定性强 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.铅蓄电池放电时,负极质量减轻,正极增重
B.升高CH3COONa溶液的温度,其水的离子积常数和pH均增大
C.CH3CH=CHCH3分子中的四个碳原子都在一条直线上
D.常温下Ksp(AgBr)=5.0×10-13,Ksp(AgCl)=1.8×10-10,则S(AgBr)>S(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素是最重要的金属元素之一,其不仅是各种钢材的主要成分,很多含铁化合物也具有重要意义。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于_________区。
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:_________。Mn2+的半径_________ Fe3+的半径(填“>”、“<”或“=”)。
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为_________(用含π的式子表示)。
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为_________;[Fe(SCN)(H2O)5]2+中Fe3+的配位数为_________,H2O中氧原子的杂化方式为_________。
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H![]() )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则C5H
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则C5H![]() 的大π键表示为________。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________(填标号)。
的大π键表示为________。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________(填标号)。
A 离子键 B 配位键 C σ 键 D 范德华力
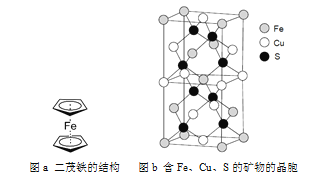
(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________。若晶胞的底面边长为A pm,高为C pm,阿伏伽德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《Journal of Energy Chemistry》报导我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:

下列说法不正确的是
A.c为电源的负极
B.a极的电极反应式为:2C2O52- -4e- =4CO2 ↑+O2↑
C.①②中,捕获CO2时碳元素的化合价均未发生变化
D.转移l mol电子可捕获CO2 11.2 L(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K层有_____________个能级,用符号表示为_____________;L层有_____________个目自级,用符号表示为_____________;M层有_____________个能级,用符号表示为_____________。由此可推知第n(n为正整数)电子层最多可能有_____________个能级,当![]() 时,能量最低的两个能级的符号分别为_____________,它们的原子轨道形状分别为_____________、_____________。
时,能量最低的两个能级的符号分别为_____________,它们的原子轨道形状分别为_____________、_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com