
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
某研究小组为测定食用白醋中醋酸的含量进行了如下操作,其中正确的是( )
A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中
B.称取4.0 g NaOH到1 000 mL容量瓶加水至刻度,配成1.00 mol·L-1 NaOH标准溶液
C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时,为滴定终点
D.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
查看答案和解析>>
科目:高中化学 来源: 题型:
新型纳米材料氧缺位铁酸盐(MFe 2Ox3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是( )
2Ox3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是( )

A.MFe2O4在与H2反应中表现了氧化性
B.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应
C.MFe2Ox与SO2反应中MFe2Ox被还原
D.若4 mol MFe2Ox与1 mol SO2恰好完全反应,则MFe2Ox中x的值为3.5
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
 (1)钢铁的腐蚀
(1)钢铁的腐蚀
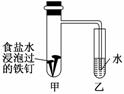
钢铁在潮湿的空气中被腐蚀的负极反应式为______________________;将经过酸洗除锈的铁钉,用饱和食盐水浸泡后,放入如图所示装置中,下列叙述正确的是________。
A.过一段时间,乙试管中的导管内水柱上升
B.甲试管中铁钉发生了化学腐蚀
C.铁钉在该装置中被腐蚀的情况随时间的延长而加快
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是________;X与过量浓硝酸反应后溶液中含有的盐的化学式为________。
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
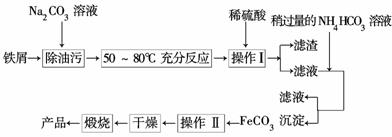
回答下列问题:
①操作Ⅰ的名称是__________________,操作Ⅱ的名称是________________;
②Na2CO3溶液可以除油污,原因是(用离子方程式表示)
________________________________________________________________________;
③请完成生成FeCO3沉淀的离子方程式:
Fe2++HCO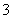 ——____________________。
——____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
新制氯水与久置的氯水相比较,下列结论不正确的是 ( )
A.颜色相同 B.前者能使有色布条褪色
C.都含有H+ D.加AgNO3溶液都能生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
试判断下面每组反应能否用同一个离子方程式表示,若能,写出相应的离子方程式;若不能,简要说明理由。
(1)CaCO3 、Na2CO3分别跟盐酸反应
(2)CuO分别跟稀硫酸、稀盐酸反应
(3)H2SO4、K2SO4溶液分别跟Ba(OH)2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
超细氧化铝是一种重要的功能陶瓷原料。
(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3,该沉淀高温分解即得超细Al2O3。NH4AlO(OH)HCO3热分解的化学反应方程式为_________________________。
(2)NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100 mL pH为2、浓度约为0.1 mol·L-1的NH4Al(SO4)2溶液,配制过程为:
①用托盘天平称量NH4Al(SO4)2·12H2O固体______________________g;
②将上述固体置于烧杯中,_________________________。
(3)在0.1 mol·L-1 NH4Al(SO4)2溶液中,铝各形态的浓度(以Al3+计)的对数(lgc)随溶液pH变化的关系见下图:
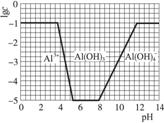
①用NaOH溶液调节(2)中溶液pH至7,该过程中发生反应的离子方程式有___________。
②请在答题卡的框图中,画出0.01 mol·L-1 NH4Al(SO4)2溶液中铝各形态的浓度的对数lgc随溶液pH变化的关系图,并进行必要标注。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com