
【题目】氯吡格雷(clopidogrel,1)是一种用于抑制血小板聚集的药物,根据不同原料,该药物合成路线通常有两条,其中以2-氯苯甲醛为原料的合成路线如下图所示:
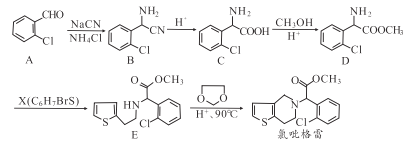
(1)分子A中非含氧官能团的名称为__________。
(2)X的结构简式为__________。
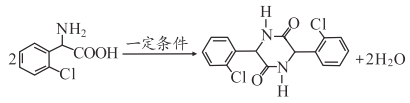
(3)分子C可在一定条件下反应生成一种含有3个六元环的产物,写出该反应的化学方程式__________。
(4)D-E的反应类型是__________。
(5)A的所有同分异构体(不包括A)中,同于芳香族化合物的有__种。
(6)已知: ![]() ,则由甲醇和乙醇为原料制备化合物
,则由甲醇和乙醇为原料制备化合物![]() 涉及的反应类型有_________ (填编号),写出制备化合物
涉及的反应类型有_________ (填编号),写出制备化合物![]() 最后一步反应的化学方程式_________。
最后一步反应的化学方程式_________。
①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应
【答案】 氯原子 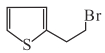
 取代反应 3 ①②③④ HOCH2CH2OH+HCHO
取代反应 3 ①②③④ HOCH2CH2OH+HCHO![]()
![]() +H2O
+H2O
【解析】(1)分子A(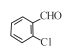 )中非含氧官能团的名称为:氯原子;(2)D与X反应生成E,根据E的结构和X的化学式可知,X的结构简式为
)中非含氧官能团的名称为:氯原子;(2)D与X反应生成E,根据E的结构和X的化学式可知,X的结构简式为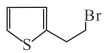 ;(3)分子C可在一定条件下反应生成一种含有3个六元环的产物,根据分析可知该反应为取代反应,反应的化学方程式为:
;(3)分子C可在一定条件下反应生成一种含有3个六元环的产物,根据分析可知该反应为取代反应,反应的化学方程式为: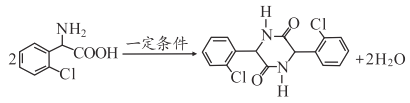 ;(4)D-E的反应,根据D、E的结构可看出除生成E以外应该还生成HBr,反应类型是取代反应;(5)芳香族化合物即含有苯环,根据A的结构可知,有位置异构和官能团异构,故符合条件的同分异构体有:
;(4)D-E的反应,根据D、E的结构可看出除生成E以外应该还生成HBr,反应类型是取代反应;(5)芳香族化合物即含有苯环,根据A的结构可知,有位置异构和官能团异构,故符合条件的同分异构体有: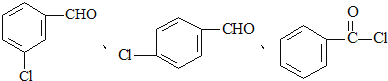 共3种;(6)
共3种;(6)
逆推法;根据信息![]() 可知,要合成
可知,要合成![]() ,首先要制得乙二醇和甲醛,乙二醇可由1,2-二溴乙烷在碱性条件下水解(取代反应)得到,1,2-二溴乙烷可由乙烯与溴水发生加成反应制得,甲醛可由甲烷催化氧化制得,图示如下:
,首先要制得乙二醇和甲醛,乙二醇可由1,2-二溴乙烷在碱性条件下水解(取代反应)得到,1,2-二溴乙烷可由乙烯与溴水发生加成反应制得,甲醛可由甲烷催化氧化制得,图示如下: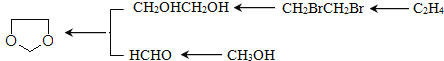 ,最后一步还涉及消去反应,综上,涉及的反应类型有①加成反应、②消去反应、③取代反应、④氧化反应,答案选①②③④;制备化合物
,最后一步还涉及消去反应,综上,涉及的反应类型有①加成反应、②消去反应、③取代反应、④氧化反应,答案选①②③④;制备化合物![]() 最后一步反应乙二醇和甲醛在浓硫酸以及加热条件下反应生成
最后一步反应乙二醇和甲醛在浓硫酸以及加热条件下反应生成![]() 和水,反应的化学方程式为:HOCH2CH2OH+HCHO
和水,反应的化学方程式为:HOCH2CH2OH+HCHO![]()
![]() +H2O。
+H2O。


科目:高中化学 来源: 题型:
【题目】(1)NaF 的水溶液呈__(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):_____,溶液中含有的各离子浓度从大到小的顺序为______。
(2)AlCl3 水溶液呈__(填“酸”、“中”、“碱”)性,把 AlCl3 溶液蒸干,灼烧,最后得到的主要固体产物是 ______。
(3)CaCl2 溶液与 Na2CO3 溶液混合可形成 CaCO3 沉淀,现将 4×10-4mol/L Na2CO3 溶液与某浓度的 CaCl2溶液等体积混合,则生成沉淀所需 CaCl2 溶液的最小浓度为__ mol·L-1(已知:KSP(CaCO3)=2.8×10-9)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.A、X、E、G、H的焰色反应均为黄色,且H为淡黄色固体.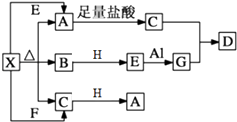
回答下列问题:
(1)写出下列物质的化学式:X , H .
(2)写出E+Al→G反应的化学方程式 , 该反应中氧化剂是 .
(3)写出G溶液中通入过量C制取D的反应离子方程式: .
(4)写出X溶液中滴加过量澄清石灰水反应的离子方程式: .
(5)0.1mol H与足量的C反应,转移的电子数为个.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物进行相互反应,生成无毒物质;或者使用新型燃料电池作汽车动力,减少汽车尾气污染.
(1)H2或CO可以催化还原NO以达到消除污染的目的.
已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJmol﹣1
2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJmol﹣1
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是 .
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率.图表示在其他条件不变时,反应:2CO(g)+2NO(g)2CO2(g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.
①该反应的△H0 (填“>”或“<”).
②若催化剂的表面积S1>S2 , 在右图中画出c (NO) 在T1、S2条件下达到平衡过程中的变化曲线 . 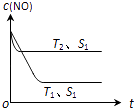
(3)在某温度时,按下列流程探究某种催化剂作用下的反应速率,用气体传感器测得不同时间的NO和CO浓度如表:![]()
时间/s | 0 | 1 | 2 | 3 | 4 |
c (NO)(×10﹣3 molL﹣1) | 1.00 | 0.50 | 0.20 | 0.10 | 0.10 |
c (CO)(×10﹣3 molL﹣1) | 3.00 | 2.50 | 2.20 | 2.10 | 2.10 |
不考虑温度变化对催化剂催化效率的影响,按要求完成以下计算(写出计算过程,只写出计算结果的不给分):①计算前2s内的△c (CO2);
②计算前2s内的平均反应速率v (N2);
③计算达到平衡时NO的转化率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关电解质溶液的叙述正确的是
A. pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
B. 等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
C. pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg2=0.3)
D. 将l0 mL pH=a的盐酸与l00 mL pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() H、
H、 ![]() H、
H、 ![]() H三种核素的性质不同
H三种核素的性质不同
B.16O2、18O2彼此是同位素
C.14N、14C两种核素的中子数相同,质子数不同
D.白磷与红磷是磷元素的两种同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,密闭容器中充入一定量的NO2和SO2 , 发生如下反应:NO2+SO2 ![]() NO+SO3 , 平衡时,下列叙述正确的是( ) ①NO和SO3 的物质的量一定相等
NO+SO3 , 平衡时,下列叙述正确的是( ) ①NO和SO3 的物质的量一定相等
②NO2和SO2的物质的量一定相等
③体系中的总物质的量一定等于反应开始时总物质的量
④SO2、NO2、NO、SO3 的物质的量一定相等.
A.①和②
B.②和③
C.①和③
D.③和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com