
A.对于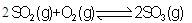  (Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ (Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ |
| B.热化学方程式中的化学计量数表示相应物质的物质的量,不能用分数表示 |
| C.需要加热才能发生的反应不一定是吸热反应 |
D.小苏打在水中的电离方程式: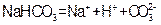 |
科目:高中化学 来源:不详 题型:单选题
| A.任何化学反应都伴随能量变化 |
| B.反应物的总能量高于生成物的总能量时,反应放热 |
| C.在铜、锌和稀硫酸构成的原电池中,铜是负极 |
| D.手机电池在充电时,是电能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放热反应在任意条件下都能自发进行 |
B.已知热化学方程式2A(g)+B(g) 2C(g)△H=-a kJ·mol-1(a>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出akJ的热量 2C(g)△H=-a kJ·mol-1(a>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出akJ的热量 |
| C.1mol·L-1的盐酸分别与1mol·L-1的氨水、1mol·L-1的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多 |
| D.BaCl2溶液中加过量H2SO4,溶液中一定不存在Ba2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CH3OH(g) ΔH=-90.8kJ·mol-1
CH3OH(g) ΔH=-90.8kJ·mol-1 CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1 CO2(g)+H2(g) ΔH=-41.3kJ·mol-1
CO2(g)+H2(g) ΔH=-41.3kJ·mol-1 CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH4 (g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H="-" 867kJ·mol-1 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)的反应热为△H3, 则△H3>△H1 |
| C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ |
| D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 kJ/mol
kJ/mol kJ/mol
kJ/mol kJ/mol
kJ/mol kJ/mol
kJ/mol查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com