
【题目】配制FeCl3溶液时,将FeCl3固体溶解在较浓的盐酸中,再加水稀释。下列说法正确的是
A.较浓盐酸可有效抑制Fe3+水解
B.稀释过程中FeCl3水解程度增大,c(H+)增大
C.FeCl3溶液中存在Fe3++3H2O=Fe(OH)3↓+3H+
D.FeCl3溶液显黄色,没有Fe(OH)3存在
【答案】A
【解析】
A项、FeCl3是强酸弱碱盐,在溶液中水解使溶液呈酸性,配制FeCl3溶液时,将FeCl3固体溶解在较浓的盐酸中,使水解平衡向逆反应方向移动,可以有效抑制Fe3+水解,故A正确;
B项、FeCl3是强酸弱碱盐,在溶液中水解使溶液呈酸性,稀释过程中FeCl3水解程度增大, n(H+)增大,但c(H+)减小,故B错误;
C项、FeCl3是强酸弱碱盐,在溶液中部分水解使溶液呈酸性,水解过程微弱,不会产生沉淀,水解的离子方程式为Fe3++3H2O![]() Fe(OH)3+3H+,故C错误;
Fe(OH)3+3H+,故C错误;
D项、FeCl3是强酸弱碱盐,在溶液中部分水解生成Fe(OH)3使溶液呈酸性,溶液中存在Fe(OH)3,故D错误;
故选A。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图有机物的正确命名为 ( )

A.2-乙基-3,3-二甲基戊烷B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷D.3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)20℃时,在烧杯中加入0.1mol/L的Na2CO3溶液,滴入酚酞呈红色。
①该溶液呈______性(填“酸”“碱”或“中”) ;
②溶液中c( Na+) ____2c(CO32-)(填“>”“<”或“=”);
③滴入酚酞呈红色的原因是___________(用离子力程式表示 )。
(2)工业上常用天然气作为制备CH3OH 的原料。已知:
CH4(g)+O2(g)=CO(g) + H2(g) +H2O(g) △H= -321.5 kJ/mol
CH4(g)+H2O(g)=CO(g)+3H2(g) △H= +250.3 kJ/mol
CO(g) +2H2(g)=CH3OH(g) △H= -90.0kJ/mol
则CH4(g)与O2(g)反应生成CH3OH(g)的热化学方程式为_________。
(3)一定温度和压强下,将2 molSO2和1mol O2置于密闭容器中发生反应2 SO2 (g)+O2(g) ![]() 2SO3(g),并达到平衡。
2SO3(g),并达到平衡。
①若升高温度,SO2的含量增大,则正反应为______ (填“放热”或“吸热”) 反应;
②若再加入1mol O2则SO2的转化率______(填“增大”或“减小”);
③若只增大压强,该反应的化学平衡常数______(填“增大”“减小”或“不变”。
(4)铅蓄电池是化学电源,其电极材料分别起Pb和PbO2,电解质溶液为稀硫酸,工作(放电)时该电池的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。试根据上述情况判断
①铅蓄电池的负极材料是_____ (填“Pb”或“PbO2”) ;
②工作时,电解质溶液的pH_____ (填“ 增大“减小”或“不变” );
③工作时,电解质溶液中阴离子移向_____极 (填“ 负”或“正” )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“酒是陈的香”是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
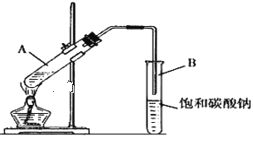
(1)装置B中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是__;饱和碳酸钠溶液的作用是___(选字母,可多选)
A.中和乙酸 B.溶解乙醇 C.降低乙酸乙酯的溶解度 D.提高产量
(2)该反应属于__(选字母,可多选)。
A.加成反应 B.取代反应 C.水解反应 D.酯化反应
(3)写出上述制取乙酸乙酯反应的化学反应方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的绝热密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0。下列不能说明该反应达到化学平衡状态的是
2NH3(g) △H<0。下列不能说明该反应达到化学平衡状态的是
A.混合气体的密度不变B.体系温度不变
C.3v逆(NH3)=2v正(H2)D.N2和NH3的浓度的比值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
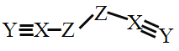
A.化合物WY是良好的耐热冲击材料
B.Y的氧化物对应的水化物可能是弱酸
C.X的氢化物的沸点一定小于Z的
D.化合物(ZXY)2中所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中含有大量氮氧化物NOx,工业脱硝技术成为研究热点。
(1)汽车尾气中NO和CO可利用车载催化剂转化为无毒物质排放。
已知:N2(g)+O2(g)=2NO(g) △H1=+183 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-565 kJ·mol-1
写出催化转化的热化学方程式_________。
(2)臭氧氧化-碱吸收法可有效脱除NO,氧化原理为:NO(g)+O3(g)![]() NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
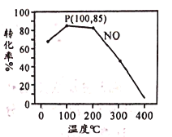
①100℃时,从开始反应到P点的平均反应速率v(NO)=__________。
②反应时同时发生副反应:2O3![]() 3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为________mol。
3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为________mol。
(3)选择性催化还原技术(NCR)可在较低温度下脱硝,原理如图I,天然锰矿可作催化剂。
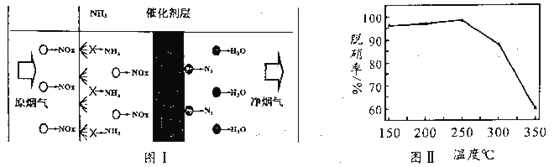
以NO代表氮氧化物,写出反应方程式_____________________;实验测得脱硝率随温度的变化如图II所示,请分析温度高于250℃时脱硝率下降的原因可能是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(如图所示),使浆液分离成固体混合物和含铬元素溶液,并回收利用。
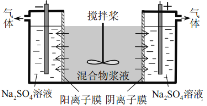
用惰性电极电解时,CrO42-能从浆液中分离出来的原因是_________________________,分离后含铬元素的粒子是__________,阴极室生成的物质为__________(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com