
【题目】(1)写出表示含有 8 个质子、10 个中子的原子的符号__________。
(2)画出 Si 原子的原子结构示意图 ________________________。
(3)写出 H2O 的电子式 ________
(4)所含元素为 18 种的周期是第________、________周期。
【答案】![]()
![]() 四 五
四 五
【解析】
(1)在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数;
(2)Si的原子序数为14,结合核外电子排布规律分析;
(3)H2O 为共价化合物,分子内共有两个氢氧共用电子对;
(4)根据元素周期表的结构回答。
(1)因质子数和中子数之和是质量数,所以O的质量数为8+10=18,,该原子的原子符号位![]() ,
,
故答案为:![]() ;
;
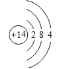
(2)Si的原子序数为14,在元素周期表第三周期IVA族,其原子结构示意图为: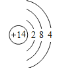 ,
,
故答案为: ;
;
(3)H2O 为共价化合物,其电子式为:![]() ,
,
故答案为:![]() ;
;
(4)在元素周期表中,共有7个周期,第七周期是不完全周期,前六周期中每个周期的元素种类数为:2、8、8、18、18和32,所以所含元素为 18 种的周期是第四和第五周期,
故答案为:四;五。


科目:高中化学 来源: 题型:
【题目】分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。下列各组中,有错误的组合是
选项 | 甲 | 乙、丙、丁 |
A | 常见干燥剂 | 浓硫酸、五氧化二磷、碱石灰 |
B | 常见合金 | 不锈钢、焊锡、生铁 |
C | 常见营养物质 | 蛋白质、维生素、无机盐 |
D | 常见碱 | 烧碱、纯碱、熟石灰 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是
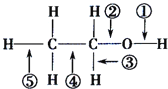
A. 与金属钠反应时,键①断裂
B. 在加热和Cu催化下与O2反应时,键①、③断裂
C. 与浓硫酸共热发生消去反应时,键②③断裂
D. 与乙酸、浓硫酸共热发生酯化反应时,键①断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯醇(CH2=CH-CH2OH)是一种无色有刺激性气味的液体,是重要的有机合成原料.请回答:
(1)丙烯醇的分子式为_______________;丙烯醇中含有的官能团的名称是________.
(2)0. 3mol丙烯醇与足量金属钠反应,能生成标准状况下的氢气_________________ L.
(3)写出丙烯醇与溴水反应的化学方程式____________________反应类型为____________
(4)丙烯醇与CH3CO18OH发生酯化反应的化方程式为:________________________________________
(5)酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确掌握化学用语是学好化学的基础.下列化学用语中不正确的是( )
A. 乙烯的结构简式CH2=CH2 B. CH4分子的球棍模型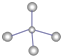
C. Ca2+的结构示意图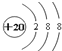 D. 乙醇的分子式C2H6O
D. 乙醇的分子式C2H6O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,反应装置略去)。注:C中为氧化铜粉末。
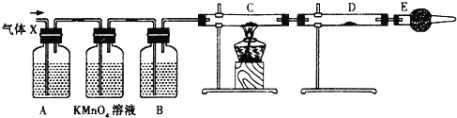
(1)实验室制备二氧化硫的化学方程式为:________________________________;
(2)乙同学认为产生氢气的理由是:______________________;
(3)B中试剂是______,D中试剂是______;(填名称)
(4)E装置的作用是_________________________;
(5)可以证明气体X中含有氢气的实验现象是:____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是( )
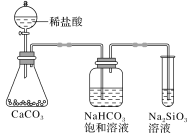
A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 已知Ra是第七周期ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强
C. 如上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com