
| 428c |
| a |
| 428c |
| a |
| 0.02cmol��214g/mol |
| ag |
| 428c |
| a |
| 428c |
| a |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 428c |
| a |
| 428c |
| a |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��ӱ�ʡʯ��ׯ�и����ڶ���ģ�������ۺϻ�ѧ�Ծ����������� ���ͣ�ʵ����
(15�֣�ij��ѧС��Ϊ�ⶨ�ӵ�����KIO3�����Ƿ������Ʊ�����KIO3,����������ʵ�顣
I .�ⶨ�ӵ�����KIO3���������������ʲ�������Ӧ��
��֪��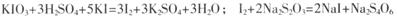
����һ��ȷ��ȡa g�ӵ��Σ����Ƴ�250 mL��Һ��
�������ȡ������Һ25.00 mL����ƿ�У���ϡ�����ữ���ټ�������KI��Һ��
���������Ե���Ϊָʾ������c mol.L-1��Na2S2O3��Һ�ζ������������Һ���յ㣬��¼���ݡ��ظ��ζ�2�Σ�ƽ������Na2S2Or��Һ12.00 mL��
(1) ����һ������250mL��Һ�õ��IJ����������ձ�������������Ͳ�⣬����____________
(2) �������е���ζ��յ�ʱ������Ϊ____________
(3) ʵ���ô˼ӵ�����KIO3����������="______" ______ (KIO3����Է�������Ϊ214)��
II.ʵ�����Ʊ�KIO3
��֪�������ο����������ڼ�����Һ�������⻯��õ���
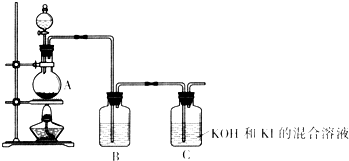
�û�ѧС��ͨ������װ���Ʊ�KIO3
(4) װ��A�з�Ӧ�����ӷ���ʽΪ____________
(5) װ��B�е��Լ�Ϊ____________
(6) д��װ��C������KIO3�����ӷ���ʽ____________��
(7) ����ʵ��װ�ô���һ������ȱ�ݣ���ָ��: __________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ӱ�ʡʯ��ׯ�и����ڶ���ģ�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
(15�֣�ij��ѧС��Ϊ�ⶨ�ӵ�����KIO3�����Ƿ������Ʊ�����KIO3,����������ʵ�顣
I .�ⶨ�ӵ�����KIO3���������������ʲ�������Ӧ��
��֪��
����һ��ȷ��ȡa g�ӵ��Σ����Ƴ�250 mL��Һ��
�������ȡ������Һ25.00 mL����ƿ�У���ϡ�����ữ���ټ�������KI��Һ��
���������Ե���Ϊָʾ������c mol.L-1��Na2S2O3��Һ�ζ������������Һ���յ㣬��¼���ݡ��ظ��ζ�2�Σ�ƽ������Na2S2Or��Һ12.00 mL��
(1) ����һ������250mL��Һ�õ��IJ����������ձ�������������Ͳ�⣬����____________
(2) �������е���ζ��յ�ʱ������Ϊ____________
(3) ʵ���ô˼ӵ�����KIO3����������=______ ______ (KIO3����Է�������Ϊ214)��
II.ʵ�����Ʊ�KIO3
��֪�������ο����������ڼ�����Һ�������⻯��õ���
�û�ѧС��ͨ������װ���Ʊ�KIO3
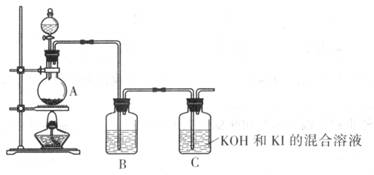
(4) װ��A�з�Ӧ�����ӷ���ʽΪ____________
(5) װ��B�е��Լ�Ϊ____________
(6) д��װ��C������KIO3�����ӷ���ʽ____________��
(7) ����ʵ��װ�ô���һ������ȱ�ݣ���ָ��: __________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�����н���ʮ�и������ϣ��������¿���ѧ�Ծ��������棩 ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com