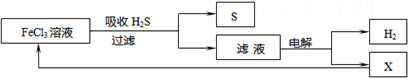
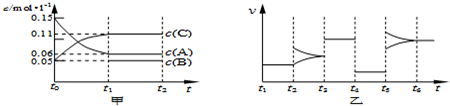(2013?浦东新区三模)向某密闭容器中加入0.15mol/L A、0.05mol/L C和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t
0时c( B)未画出,t
1时增大到0.05mol/L].乙图为 t
2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况.
(1)若t
4时改变的条件为减小压强,则B的起始物质的量浓度为
0.02
0.02
mol/L;该反应的平衡常数表达式为K=
.
(2)若t
5时改变的条件是升温,此时v(正)>v(逆),平衡常数K的值将
增大
增大
(选填“增大”、“减小”或“变”).
(3)若 t
1=15s,则t
0~t
1阶段以C 浓度变化表示的平均反应速率为v(C)=
0.004
0.004
mol/L?s.t
3 时改变的某一反应条件可能是
ab
ab
(选填序号).
a.使用催化剂 b.增大压强 c.增大反应物浓度 d.降低产物浓度
(4)若A的物质的量减少0.02mol时,容器与外界的热交换总量为a kJ,写出该反应的热化学方程式
3A(g)?B(g)+2C(g)△H=+150akJ?mol-1
3A(g)?B(g)+2C(g)△H=+150akJ?mol-1
.