
 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )A、 |
B、 |
C、 |
D、 |
科目:高中化学 来源: 题型:
| ||
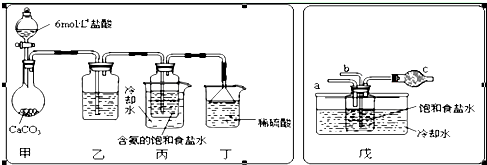
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、NO3- |
| B、使pH试纸显深蓝色的溶液:Cu2+、NO3-、Fe3+、SO42- |
| C、由水电离产生的c(OH-)=1×10-14mol/L的溶液:Ba2+、Na+、NO3-、Cl- |
| D、所含溶质为Na2SO4的溶液:K+、SiO32-、NO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CS2为V形分子 |
| B、NCl3的空间构型为平面三角形 |
| C、铝的第一电离能比镁的第一电离能大 |
| D、SiF4和H2O的中心原子均为sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:

A、它的单体是 |
B、丁苯橡胶是CH2═CH-CH═CH2和 通过缩聚反应制得的 通过缩聚反应制得的 |
| C、装液溴或溴水的试剂瓶可用丁苯橡胶作瓶塞 |
| D、丁苯橡胶会老化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Na+、SO32-、Cl- |
| B、K+、Na+、Cl-、SO42- |
| C、K+、Na+、Cl-、AlO2- |
| D、K+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3溶液中存在:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
| B、室温下,向0.01mol?L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、Na2CO3溶液:c(OH-)+c(HCO3-)=c(H+)+2c(H2CO3) |
| D、25℃时,Al(OH)3固体在20mL 0.01mol/L氨水中的Ksp比在20mL 0.01mol/LNH4Cl溶液中的Ksp小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com