
����Ŀ�����������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ����
A. ��֪2SO2(g)+O2��g��![]() 2SO3(g)Ϊ���ȷ�Ӧ����SO2������һ������SO3������
2SO3(g)Ϊ���ȷ�Ӧ����SO2������һ������SO3������
B. ��֪C(ʯī,s)��C(���ʯ,s) ��H��0������ʯ��ʯī�ȶ�
C. ��֪H+(aq)+OH�C(aq)��H2O��1�� ��H = -57.3kJ��mol-1�����κ�����к͵ķ�Ӧ�Ⱦ�Ϊ57.3kJ
D. һ��������2SO2(g)+O2(g) ![]() 2SO3(g) ��H1 ��2SO2(g)+O2(g)
2SO3(g) ��H1 ��2SO2(g)+O2(g) ![]() 2SO3(l) ��H2 ����H1>��H2
2SO3(l) ��H2 ����H1>��H2
���𰸡�D
��������
A. ���ݻ�ѧ��Ӧ�Ƿ��ȷ�Ӧ����Ӧ����������������������������
B. ʯī��ȫת��Ϊ���ʯʱ��Ҫ����������˵�����ʯ��������ʯī������Խ��Խ�ȶ���
C. ��ϡ��Һ��ǿ���ǿ�Ӧ����1 molˮ�ų�������Ϊ�к��ȣ�
D. 2 mol��̬SO3��2 molҺ̬SO3�������ߣ��������2 mol��̬SO3ʱ�ų��������٣��ʱ��
A. ���ݻ�ѧ��Ӧ�Ƿ��ȷ�Ӧ��2mol���������1mol��������֮����2mol�������������������ȷ������������������������Ĺ�ϵ����A�����
B. ʯī��ȫת��Ϊ���ʯʱ��Ҫ����������˵�����ʯ��������ʯī������Խ��Խ�ȶ�������ʯī�Ƚ��ʯ�ȶ�����B�����
C. ��ϡ��Һ��ǿ���ǿ�Ӧ����1molˮ�ų�������Ϊ�к��ȣ���H=57.3 kJ/mol���������ʱ���ȣ����Էų�������С��57.3 kJ/mol����C�����
D. 2 mol��̬SO3��2 molҺ̬SO3�������ߣ��������2 mol��̬SO3ʱ�ų��������٣��ʱ����H1����H2����D����ȷ��
��ѡD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ʵ���������Fe��ˮ������Ӧ��ʵ��,ʵ��װ����ͼ�ס�����ʾ��

��֪B�з������������ʯ���Ļ���C�зŵ��Ǹ������EΪ�ƾ���ƣ�G Ϊ������˿���ֵľƾ��ơ��Ա���װ�ã��ش���������:
��1����μ����װ�õ�������?________________��
��2����װ����ʪɳ�ӵ�������________________��
��3��B��������Ӧ�Ļ�ѧ����ʽΪ_________________��
��4����ͬѧ��Ϊ������װ�õĵ��ܿڴ���ȼ��Ӧ���������壬װ��H�ز����٣�H��������________________��
��5���Աȼס�����װ�õ�B��K��B���ŵ���____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�������ǵ�����ϢϢ��ء��ش��������⣺
��1�������ƣ�Na2[Fe(CN)5(NO)] 2H2O�����������Ƽ�������˥�ߡ�
��Fe3+�ļ۵��ӹ����ʾʽΪ____________��
���������в����ڵ���������____________������ţ���
a�����Ӽ� b�������� c����λ�� d�����Թ��ۼ� e���Ǽ��Թ��ۼ� f�����
�������Ƶ��ڽ�[Fe(CN)5(NO)]2-�У��ǽ���Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ______������������Ԫ�ذ�ԭ�Ӹ�����Ϊ1:3��ɵij��������ӵĿռ乹��Ϊ_________��
��2�����Ȼ�����һ����Ҫ�����Σ��۷е�ϵͣ������ڱ�ͪ��
��FeCl3��������Ϊ____________��
��FeCl3���۵�(555K)����AlCl3(467K)��ԭ����_______________��
��Fe3+����KSCN��Һ���飬SCN-�������������ĸ�����Ϊ_______��
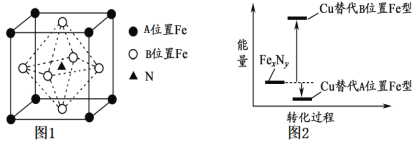
��3��ijFexNy�ľ�������ͼ1��ʾ���仯ѧʽΪ____________��Cu����ȫ����þ����е�Aλ��Fe��Bλ��Fe���γɲ���Fe(x-n)CunNy��FexNyת��Ϊ����Cu����Ͳ���������仯����ͼ2��ʾ�����и��ȶ���Cu����Ͳ��ᄃ����ܶ�Ϊ�� gcm-3�������ӵ�����ΪNA��������a=___nm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���棨Ce)��һ����Ҫ��ϡ��Ԫ�ء��Ը���CeO2�ķϲ�����ĩ����SiO2�� Fe2O3�Լ���������������ϡ������ʣ�Ϊԭ�ϣ����ö��ַ��������档��ش��������⣺
(1)ʪ������������������IJ����������£�

��֪��CeO2������ϡ���ᣬҲ������NaOH��Һ��
�����ijɷ���________����Ӧ�ڵ����ӷ���ʽ��________��
(2)�ɷ������������������ǰ�Ce(OH)3������������Ce(OH)4�����������з����Ļ�ѧ��Ӧ����ʽΪ________�������Ʊ�Ge(OH)4���������±���
�ɷ����������� | �����¶�/�� | ������/% | ����ʱ��/h |
��¶������ | 110120 | 90 | 18 |
�ڶ�����������¯�� | 110120 | 99 | 8 |
�ڶ�����������¯�д����������ʱ���ԭ����________��
(3)���õ�ⷽ��Ҳ����ʵ����Ļ��ա�
�������������µ��Ce2O3 (��ͼ���������缫��ӦʽΪ______�����ӽ���ĤΪ______ (���������������������ӽ���Ĥ��
�ڵ�����Ce(SO4)2����Ҫ����������������ɱ���Һ���������������ܲⶨ��ҵ����NaNO2�ĺ�����д��������Ӧ�����ӷ���ʽ_______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±��г��ˢ١������Ԫ�������ڱ��е�λ�ã�
��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 | |
1 | �� | |||||||
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� |
�밴Ҫ��ش��������⡣
��1��Ԫ�آܵ�������______��Ԫ�آ������ڱ�������λ��___________����Ԫ��ԭ�ӵ�ʧ���ӵĽǶȿ���Ԫ�آܾ���____________(������ԡ���ԭ�ԡ�)��
��2������̬�⻯����ȶ���������ǿ��˳�����У��ޢܢߵ��⻯���ȶ��ԣ�_____________________(д�⻯��Ļ�ѧʽ)��
��3��Ԫ�آߵ�ԭ�ӽṹʾ��ͼ��____________��
��4��д��Ԫ�آ��γɵĵ�����������ȼ�յĻ�ѧ����ʽ________________����һ��Ӧ��___________(����ȡ����ȡ�)��Ӧ��
��5���õ���ʽ��ʾ����ᷴӦ�õ��Ļ�������γɹ���_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ����Ҫ������Cu�Ļ������ڿ�ѧ�о���ҵ�����о���������;����CuSO4��Һ���������Һ�����Һ�ȡ���ش��������⣺
��1��CuSO4���ɽ���ͭ��Ũ���ᷴӦ�Ʊ����÷�Ӧ�Ļ�ѧ����ʽΪ___________��
��2��CuSO4��ĩ����������һЩ�л����е���ˮ�֣���ԭ����_______��
��3��SO42-�����幹����________������Sԭ�ӵ��ӻ����������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����HgCl2��������ľ�ĺͽ��ʱ걾�ı��桢Ƥ�����ƺ�����ʴ���Ƿ�����ѧ����Ҫ�Լ��������������ͷ�������
��1����HgCl2��ˮ������ˮ�⣺HgCl2+H2O![]() Hg(OH)Cl+HCl��Ϊ������������Ӧ����HgCl2��ˮ�⣬���Բ�ȡ�Ĵ�ʩ��_________����ѡ���ţ�
Hg(OH)Cl+HCl��Ϊ������������Ӧ����HgCl2��ˮ�⣬���Բ�ȡ�Ĵ�ʩ��_________����ѡ���ţ�
a. ��ˮϡ�� b. ����HCl��Ũ�� c. ��ʱ���߲��� d. ����
��HgCl2��ϡ��ˮ��Ӧ���������ܽ�İ����Ȼ�������ѧ����ʽΪ��HgCl2+2NH3��Hg(NH3)Cl��+NH4Cl��������Ӧ�Ķ�����Ԫ���У��ǽ�������ǿԪ��ԭ�ӵ����������Ų�ʽΪ_______����ԭ�Ӻ����������______�ֲ�ͬ����չ����
��2����֪PCl3��NH3���ӽṹ���ƣ�PCl3�ĵ���ʽ��________��PCl3��NH3�ķе�Ƚϣ�_____�ߣ���ԭ����_____________��
��3������һ���⻯��HN3�������л��ϳɣ���������������ƣ���HN3�백ˮ��ϣ��˷�Ӧ�Ļ�ѧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2NO2(g)![]() 2NO(g)+O2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־��
2NO(g)+O2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־��
����λʱ��������1 mol O2��ͬʱ����2 mol NO2
����λʱ��������1 mol O2��ͬʱ����2 mol NO
����NO2��NO��O2��ʾ�ķ�Ӧ����֮��Ϊ2��2��1��״̬
������������ɫ���ٸı��״̬ �����������ܶȲ��ٸı��״̬
����������ѹǿ���ٸı��״̬ ����������ƽ����Է����������ٸı��״̬
A. �٢ܢޢ� B. �ڢۢݢ� C. �٢ڢۢܢ� D. ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С���ŵ㣮һ����Һ̬�£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������KOH��Һ��Ϊ�������Һ�����й��ڸõ�ص���������ȷ���ǣ� ��

A.a���ķ�Ӧʽ��N2H4+4OH����4e���TN2��+4H2O
B.�ŵ�ʱ�����Ӵ�a��������������b��
C.�õ�س����ŵ�ʱ�����ӽ���Ĥ��ѡ�������ӽ���Ĥ
D.��·��ת�Ƶ���3NAʱ��������16.8 L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com