
【题目】三草酸合铁酸钾晶体(K3[Fe(C2O4)3]xH2O)是一种光敏材料,在110℃可完全失去结晶水.为测定该晶体中铁的含量,某实验小组做了如下实验:铁含量的测定
步骤一:称量5.00g三草酸合铁酸钾晶体,配制成250mL溶液.
步骤二:取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO ![]() 被还原成Mn2+ . 向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
被还原成Mn2+ . 向反应后的溶液中加入一小匙锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO ![]() 被还原成Mn2+ . 重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液分别为19.98mL和20.00mL.请回答下列问题:
被还原成Mn2+ . 重复步骤二、步骤三操作,滴定消耗0.010mol/L KMnO4溶液分别为19.98mL和20.00mL.请回答下列问题:
(1)滴定过程中,高锰酸钾应盛装在滴定管中(填“酸式”或“碱式”).
(2)用离子方程式表示步骤二中涉及到的相关化学反应:;Zn+2Fe3+═2Fe2++Zn2+ .
(3)步骤三中滴定终点的判定: .
(4)在步骤二中,若加入的KMnO4溶液的量不够,则测得的铁含量 . 在步骤三中,若滴定前仰视读数,滴定后俯视读数,则测得的铁含量 . (选填“偏低”、“偏高”、“不变”)
(5)实验测得该晶体中铁的质量分数为 .
【答案】
(1)酸式
(2)2MnO ![]() +5C2O
+5C2O ![]() +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
(3)当最后一滴高锰酸钾加入后,溶液颜色变为紫红(浅红色)色,且半分钟内不褪色
(4)偏高;偏低
(5)11.2%
【解析】解:(1)高锰酸钾具有强氧化性,能腐蚀橡皮管,所以用酸式滴定管盛放,所以答案是:酸式;(2)取所配溶液25.00mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO ![]() 被还原成Mn2+ , 结合原子守恒和电荷守恒写出反应的离子方程式为:2MnO
被还原成Mn2+ , 结合原子守恒和电荷守恒写出反应的离子方程式为:2MnO ![]() +5C2O
+5C2O ![]() +16H+=2Mn2++10CO2↑+8H2O,(3)当滴入最后一滴KMnO4溶液,溶液无色变为紫红色且半分钟不褪色,则达到了滴定终点,所以答案是:当最后一滴高锰酸钾加入后,溶液颜色变为紫红(浅红色)色,且半分钟内不褪色;(4)若在步骤二中滴入酸性高锰酸钾溶液不足,则会有部分草酸根离子未被氧化,在步骤三中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高,在步骤三中,若滴定前仰视读数,滴定后俯视读数,读取标准溶液的体积减小,则测得的铁含量偏低,所以答案是:偏高;偏低;(5)根据离子方程式计算,5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O, n(Fe)=5n(MnO
+16H+=2Mn2++10CO2↑+8H2O,(3)当滴入最后一滴KMnO4溶液,溶液无色变为紫红色且半分钟不褪色,则达到了滴定终点,所以答案是:当最后一滴高锰酸钾加入后,溶液颜色变为紫红(浅红色)色,且半分钟内不褪色;(4)若在步骤二中滴入酸性高锰酸钾溶液不足,则会有部分草酸根离子未被氧化,在步骤三中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高,在步骤三中,若滴定前仰视读数,滴定后俯视读数,读取标准溶液的体积减小,则测得的铁含量偏低,所以答案是:偏高;偏低;(5)根据离子方程式计算,5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O, n(Fe)=5n(MnO ![]() )=5×
)=5× ![]() ×0.01×10﹣3×10=1.0×10﹣2mol, m(Fe)=56 gmol﹣1×1.0×10﹣2mol=0.56g.晶体中铁的质量分数=
×0.01×10﹣3×10=1.0×10﹣2mol, m(Fe)=56 gmol﹣1×1.0×10﹣2mol=0.56g.晶体中铁的质量分数= ![]() ×100%=11.2%,所以答案是:11.2%;
×100%=11.2%,所以答案是:11.2%;


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作叙述正确的是( )
A. 萃取操作必须在漏斗中进行
B. 振荡试管中液体时,手拿住试管,用手腕甩动
C. 用剩的药品应收集起来,放回原试剂瓶中
D. 称量物质时,先取小砝码,再依次取较大的砝码
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名的“侯氏制碱法”的第一步反应是向饱和食盐水中通入CO2而析出NaHCO3 , 该反应可表示为:NH3+NaCl+CO2+H2O═NaHCO3↓+NH4Cl
已知NaCl、NaHCO3、NH4Cl如下温度的溶解度:
物质 | NaCl | NaHCO3 | NH4Cl |
40℃时溶解度/g | 37 | 13 | 46 |
10℃时溶解度/g | 33 |
今在40℃时,向434g饱和食盐水中通入44.8L(标准状况)NH3 , 再向溶液中通入过量的CO2 , 求:
(1)可析出NaHCO3多少克?
(2)NH4Cl能否析出?
(3)若降温至10℃,可析出NH4Cl多少克?
(4)降温至10℃时,若要析出更多的NH4Cl晶体应采取什么措施?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题: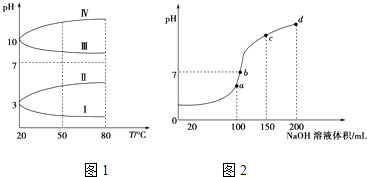
(1)NH4Al(SO4)2可作净水剂,其理由是(用必要的化学用语和相关文字说明).
(2)如图1是0.1molL﹣1电解质溶液的pH随温度变化的图象.①其中符合0.1molL﹣1NH4Al(SO4)2的pH随温度变化的曲线是(填写序号);
②20℃时,0.1molL﹣1NH4Al(SO4)2中2c(SO ![]() )﹣c(NH
)﹣c(NH ![]() )﹣3c(Al3+)=(要求填精确的表达式)
)﹣3c(Al3+)=(要求填精确的表达式)
(3)室温时,向100mL 0.1molL﹣1NH4HSO4溶液中滴加0.1molL﹣1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大的是;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合物的代数和为6;R和Q可形原子数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应.请回答下列问题:
(1)T元素在期表中的位置是________;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为________(写出其中一种物质的名称).
(2)X、Z、Q三种元素的原子半径由小到大顺序为________(填元素符号).
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为________.
(4)下列可以判断R和T金属性强弱的是________(填序号).
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为________;R2Q2与X2Q反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃、101 kPa的条件下,断裂1 mol H—H键吸收436 kJ能量,断裂1 mol Cl—Cl键吸收243 kJ能量,形成1 mol H—Cl键放出431 kJ能量。H2+Cl2===2HCl的化学反应可用下图表示:
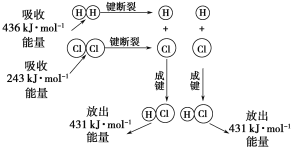
请回答下列有关问题:
(1)反应物断键吸收的总能量为________。
(2)生成物成键放出的总能量为________。
(3)判断H2+Cl2===2HCl是________(填“吸收”或“放出”)能量。
(4)反应物的总能量________(填“>”,“=”或“<”)生成物的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的有
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计的水银球靠近蒸馏烧瓶的瓶底
C. 过滤时,玻璃棒下端在引流过程中应靠在三层滤纸处
D. 称量时,称量物放在纸上置于托盘天平左盘,砝码直接放在天平右盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】平达喜是一种常用抗酸药,其主要成分是由短周期元素组成的化合物X,式量为602.甲同学欲探究X的组成.查阅资料:
①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、碱式碳酸镁铝(或结晶水合物).
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全.
实验过程:
Ⅰ.向一定量的X粉末中加入45.0 mL的2mol/L盐酸溶液中,恰好完全反应并收集到112 mL(标准状况下)的A气体,A气体可使澄清石灰水变浑浊.
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰.
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤.
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解.
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C.沉淀物进行洗涤干燥后重1.74 g.
(1)A的电子式是 .
(2)由Ⅰ中可确定X中存在两种带负电荷的原子团及个数比 .
(3)由Ⅰ判断X一定不含有的元素是 .
(4)Ⅲ中生成B的离子方程式是 .
(5)Ⅳ中B溶解的化学方程式是 .
(6)沉淀C的化学式是 .
(7)若X中n(B):n(C)=1:3,则X的化学式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com