
| A. | 苯和甲苯不互为同系物 | B. | 淀粉和纤维素互为同分异构体 | ||
| C. | 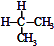 与 与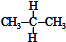 互为同分异构体 互为同分异构体 | D. | 异丁烷与2-甲基丙烷互为同种物质 |
分析 A.结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
B.淀粉、纤维素的分子式不一定相同;
C.甲烷是正四面体结构;
D.异丁烷就是2-甲基丙烷.
解答 解:A.苯和甲苯结构相似,分子组成相差1个“CH2”原子团,故互为同系物,故A错误;
B.淀粉、纤维素都为高聚物,n介于较大的范围之间,不确定,则二者的分子式不一定相同,则不是同分异构体,故B错误;
C.甲烷是正四面体结构,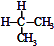 与
与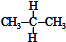 是同种物质,故C错误;
是同种物质,故C错误;
D.异丁烷就是2-甲基丙烷,是同种物质,故D正确.
故选D.
点评 本题考查同系物、同分异构体的概念分析、比较,难度不大,注意概念的理解与应用,把握“五同”是指同位素、同素异形体、同系物、同分异构体、同种物质,注意从相同的内容、不同的内容、使用范围等方面掌握判断的方法和技巧.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:| 组别 | a | b | c中的溶质 |
| 甲 | C | C | KOH |
| 乙 | Cu | Cu | NaCl |
| 丙 | Cu | Cu | CuSO4 |
| 丁 | C | C | NaCl |
| A. | 甲实验中溶液的pH要变小,两极均有气体放出 | |
| B. | 乙实验中发生反应的总反应式为:Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$ Cu(OH)2↓+H2↑ | |
| C. | 丙实验中c溶液的浓度不变,a极质量增大 | |
| D. | 丁实验中a极电极反应式为:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素和高级脂肪酸都是高分子化合物 | |
| B. | 天然油脂一般为多种混甘油酯的混合物,因此无固定的熔沸点 | |
| C. | 皂化反应完成后加入食盐可以使高级脂肪酸钠从混合物中析出,这一过程叫盐析 | |
| D. | 区别植物油和矿物油的正确方法是将它们分别加入氢氧化钠溶液,加热、振荡,观察是否分层 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴入石蕊试液 | |
| B. | 加入金属钠 | |
| C. | 加入银氨溶液(微热) | |
| D. | 加入氢氧化钠溶液后加热蒸馏,在馏出物中加入银氨溶液(微热) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ①②④⑤ | D. | ①②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下与水反应生成酸 | B. | 高温时能与纯碱反应 | ||
| C. | 熔点高,硬度大 | D. | 常温下能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 暖冰中水分子是直线型分子 | |
| B. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| C. | 暖冰中水分子是分子密堆积 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com