
| A.①②③ | B.①④⑤ | C.②④⑤ | D.②⑤ |


科目:高中化学 来源:不详 题型:单选题
| A.离子半径:Na+>Al3+>F- |
| B.热稳定性:HCl>PH3>AsH3 |
| C.酸性:H3PO4>H2CO3>H2SiO3 |
| D.熔点:CH3(CH2)3CH3>(CH3)2CHCH2CH3>CH3C(CH3)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.其氯化物是离子化合物 |
| B.其最高价氧化物水化物为一种弱碱 |
| C.它比Na更易置换水中的氢 |
| D.它的碳酸盐难溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 电离能/(kJ?mol-1) | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:HClO4>H2SO4>H3PO4 |
| B.金属性:Na>Mg>Al |
| C.原子半径:r(S)>r(O)>r(F) |
| D.稳定性:HI>HBr>HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性H4SiO4<H3PO4<H2SO4<HClO4 |
| B.碱性Ca(OH)2>Mg(OH)2>Al(OH)3 |
| C.稳定性SiH4>NH3>H2O>HF |
| D.半径O2->F->Mg2+>Al3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
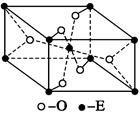
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
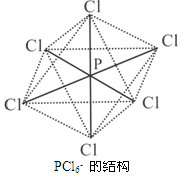
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com