
【题目】下列关于某些离子的检验说法中正确的是
A.向某溶液中加稀盐酸,能产生澄清石灰水变浑浊的无色、无味的气体,则该溶液中一定有CO32-
B.向某溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶液中一定有SO42-
C.向某溶液中加入浓NaOH溶液并加热,能产生使湿润的红色石蕊试纸变蓝的气体,则该溶液一定有NH4+
D.向某溶液中加入AgNO3溶液产生白色沉淀,则该溶液中一定含有Cl-
【答案】C
【解析】
A. 使澄清石灰水变浑浊的无色、无味的气体为CO2,与盐酸反应能产生CO2气体,则该溶液中可能存在CO32-、HCO3-,故A错误;
B. 若溶液中存在Ag+,则加入BaCl2溶液时有白色AgCl沉淀产生,再加盐酸,沉淀不消失,所以上述实验不能说明一定有SO42-,还可能存在Ag+,故B错误;
C. 能使湿润的红色石蕊试纸变蓝的气体为氨气,溶液中加入浓NaOH溶液并加热产生氨气,则该溶液一定有NH4+,反应为NH4++OH-![]() NH3↑+H2O,故C正确;
NH3↑+H2O,故C正确;
D. Ag2CO3也难溶于水,所以若溶液中含有CO32-,加入AgNO3溶液时会产生白色沉淀,则该溶液中不一定含有Cl-,故D错误;
故选C。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】实验室常用的几种气体发生装置如图A、B、C所示:
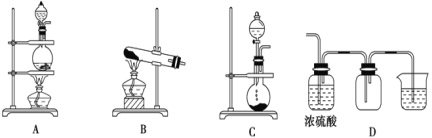
(1)实验室用熟石灰和氯化铵固体制取氨气,应选择____装置,检验该装置气密性的操作方法是_________________。
(2)气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是____(填序号,下同)。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的____。
① CO2 ② H2 ③ Cl2
Ⅰ.写出A装置中反应的离子方程式___________________________。
Ⅱ.D装置中小烧杯中应盛放____,目的是_________________。
Ⅲ.若要收集干燥纯净的X气体,上述装置应如何改进:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】每年10月23日上午6:02到晚上6:02倍誉为“摩尔日”(Mole Day),这个时间的美式写法为6:02 10/23,外观与阿伏伽德罗常数6.02×1023相似。设NA为阿伏伽德罗常数的值,下列说法正确的是
A.7.8g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1NA
B.1L0.1mol·L-1碳酸钠溶液中含有的氧原子数为0.3NA
C.将100mL 0.1mol·L-1FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数为0.01NA
D.将CO2通过0.1mol Na2O2时,反应共转电子数为移0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①乙醇 ②铜 ③CaO ④CO2 ⑤食醋 ⑥Ba(OH)2⑦红褐色氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩硫酸铁
(1)按物质的分类方法填写表格的空白处:
分类标准 | _______ | 氧化物 | _____ | _____ | 电解质 | 非电解质 |
物质 | ② | _____ | ⑤⑧⑨ | ⑦ | _____ | _____ |
(2)上述十种物质中有两种物质之间可发生离子反应:OH-+ H+=H2O,该反应对应的化学方程式为________________________________。
(3)少量的②加入的溶液中反应⑩的离子方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A.7.8g Na2O2中含有的离子总数为 0.4NA
B.标准状况下,22.4L 乙醇所含的分子数为0.1NA
C.常温常压下,0.18g H2O所含的电子数为0.1NA
D.常温常压下,3.2g O2所含的氧原子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量的铜与100mL某浓度的硝酸反应,铜完全溶解时,产生标准状况下的NO和NO2混合气体11.2L。待产生的气体全部释放后,向溶液中加入140mL 5mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度是
A.7mol·L-1B.9mol·L-1C.10mol·L-1D.12mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蓄电池放电、充电时反应为:Fe + Ni2O3 +3H2O![]() Fe(OH)2 +2Ni(OH)2 ,下列推断不正确的是( )
Fe(OH)2 +2Ni(OH)2 ,下列推断不正确的是( )
A.放电时,负极上的电极反应式是:Fe+2OH--2e-=Fe (OH)2
B.放电时,每转移2 mol 电子,正极上有1 mol Ni2O3 被氧化
C.充电时,阳极上的电极反应式是:2Ni(OH)2 -2e-+ 2OH- = Ni2O3 +3H2O
D.该蓄电池的电极必须是浸在某种碱性电解质溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用“化学计量在实验中的应用”的相关知识进行填空(设 NA 表示阿伏加德罗常 数的值)。
(1)标准状况下,0.2 mol 氨气的体积是_______________,含氢原子数是_______________。
(2)H2SO4 的摩尔质量是_______________, 49 g 的 H2SO4 中含有_______________mol 氧原子,能与_______________mol NaOH 恰好完 全反应。
(3)将 0.5 mol Na2CO3溶解在水中,配成 500mL 溶液,所得溶液中溶质的物质的量浓度是 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】局部麻醉药普鲁卡因E(结构简式为![]() )的三条合成路线如下图所示(部分反应试剂和条件已省略):
)的三条合成路线如下图所示(部分反应试剂和条件已省略):

完成下列填空:
(1).比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是___________。
(2).写出反应试剂和反应条件。反应①______;③______
(3).设计反应②的目的是____________。
(4).B的结构简式为_____;C的名称是____。
(5).写出一种满足下列条件的D的同分异构体的结构简式____。
①芳香族化合物 ②能发生水解反应 ③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗_____mol NaOH。
(6).普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com