
����Ŀ���о�NO2��NO��CO��Ⱦ�ﴦ�����Խ��������й�������Ҫ���塣
��1����NO2(g)+CO(g)==CO2(g)+NO(g)��H1=-234.00kJ/mol
��1/2N2(g)+1/2O2(g)=NO(g)��H2=-89.75kJ/mol
��2NO(g)+O2(g)==2NO2(g)��H3=-112.30kJ/mol��
��NO2�����CO���巴Ӧ��������Ⱦ���������Ȼ�ѧ����ʽΪ______________��
��2��ij�¶��£���10L�ܱ������зֱ����0.1molNO2��0.2molCO��������Ӧ��2NO2(g)+4CO(g)=N2(g)+4CO2(g)����10min��Ӧ�ﵽƽ����������ѹǿ��Ϊԭ����![]() ��
��
��0��10min����CO��ƽ����Ӧ����v(CO)=__________��
���������й۲쵽_____�����жϸ÷�Ӧ�ﵽƽ��״̬��
��Ϊ������Ⱦ�ﴦ��Ч�ʣ���ʼ���Ͷ�ϱ�Ϊ______��
��ƽ�����CO��CO2����Ũ�ȷֱ�����һ������ƽ��_____(���������������������������ƶ���)��

��3���ڸ�Ч������������NH3��ԭNO2������Ⱦ�ﴦ����
����ͬ�����£�ѡ��A��B��C���ִ������з�Ӧ�����ɵ��������ʵ�����ʱ��仯��ͼa�������С����______(��E(A)��E(B)��E(C)��ʾ���ִ����¸÷�Ӧ���)��
���ڴ���A�����²����ͬʱ�䴦��NO2�������¶ȹ�ϵ��ͼb����˵��ͼ��������������С��ԭ��________(������¶ȷ�Χ�ڴ�Ч����ͬ)��

��4�����������ں���NO2��������ˮ�м�����������۵Ķ����̿��������ˮ�ľ������Խ�ϵ缫��Ӧ˵�������̿����Ҫ����_____��
���𰸡� 2NO2(g)+4CO(g)=4CO2(g)+N2(g) ��H=-868.8kJ/mol 4��10-4mol/(L.min) ��ϵ��������ɫ���ٸı� ![]() ���ƶ� E(A) ����300�棬��Ӧδ�ﵽƽ�⣬�¶���������Ӧ���ʼӿ�������300�棬��Ӧ��ƽ�������¶���������Ӧ������� ����̿���������γɵ�ԭ�������������������Ӧ2NO2+8H++8e-=N2��+4H2O����NO2ת��Ϊ����Ⱦ����N2
���ƶ� E(A) ����300�棬��Ӧδ�ﵽƽ�⣬�¶���������Ӧ���ʼӿ�������300�棬��Ӧ��ƽ�������¶���������Ӧ������� ����̿���������γɵ�ԭ�������������������Ӧ2NO2+8H++8e-=N2��+4H2O����NO2ת��Ϊ����Ⱦ����N2
����������1����Ӧ�١�4���ڡ�2���ۡ�1�õ���2NO2(g)+4CO(g)=4CO2(g)+N2(g) ��H=-868.8kJ/mol��
��2�� 2NO2(g) + 4CO(g) = N2(g) + 4CO2(g)
��ʼ�� 0.1 0.2 0 0
��Ӧ�� x 2x x/2 2x
ƽ���� 0.1��x 0.2��2x x/2 2x
���º���ѹǿ�ıȵ�����������ʵ����ıȣ�����![]() �����x=0.02mol��
�����x=0.02mol��
�����ϲμӷ�Ӧ��COΪ0.04mol����Ӧ����Ϊ![]() = 4��10-4mol/(L.min)��
= 4��10-4mol/(L.min)��
�ڷ�Ӧ��ƽ���Ժ��������ʵ�Ũ�ȶ����仯����ΪNO2��Ũ�Ȳ��䣬������ϵ����ɫӦ��Ҳ���仯����۲쵽��ɫ���䣬֤����Ӧ��ƽ�⡣
��Ϊ������Ⱦ�ﴦ��Ч�ʣ�Ӧ�ñ�֤��Ӧ����ת��Ϊ�������������Ӧ�ﶼ��������������ʼ���Ͷ�ϱ�Ϊ![]() ��
��
�ܴ�ƽ��ʱһ����Q=K�����ڽ���CO��CO2����Ũ�ȷֱ�����һ������Ϊ���ߵ�ϵ����ȣ���һ���ڷ���һ���ڷ�ĸ������Ũ���̵ı�ֵQ���䣬��Q��Ȼ����K����Ӧƽ�ⲻ�ƶ���
��3����һ����˵����Ӧ�Ļ��ԽС����Ӧ������Խ�죬����E(A)��С��
������Ϊ�ڴ���A�����²����ͬʱ�䴦��NO2�������¶ȹ�ϵ���������ϵĵ㲻һ������ƽ��̬����Ӧ��������ʱ��ʱ��β��ܴ�ƽ�⣬������Խ�죬��Ӧ����Խ�ࣻ��Ӧ���ʺܿ��ʱ��Ӧ��ƽ�⣬���¶�Խ�ߣ�ƽ�������ƶ�����Ӧ�������١�����ԭ��Ϊ������300�棬��Ӧδ�ﵽƽ�⣬�¶���������Ӧ���ʼӿ�������300�棬��Ӧ��ƽ�������¶���������Ӧ������С�
��4�������������������ԭ��أ���������̼�������ԭ��ص������缫����Ϊ������̼Ϊ�����������Ӧ�÷���NO2�õ���ת��Ϊ�����ķ�Ӧ�����Է���ʽΪ��2NO2+8H++8e-=N2��+4H2O��


 ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��Cu- Li�ɳ���صĹ���ԭ����ͼ��ʾ�����з�ˮϵ���Һ��ˮϵ���Һ������ӹ��������մ�Ƭ( LISICON)����������˵����ȷ����
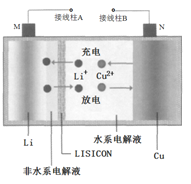
A. �մ�Ƭ����ˮ����ͨ��
B. ��طŵ�ʱ��N���Ϸ���������Ӧ
C. ��س��ʱ��������BӦ�����ֱ����Դ�ĸ�������
D. ��س��ʱ��������ӦΪLi++e-=Li
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��ȼ�ռ������������ȼ�������ʡ���ѧ��ȼ�ռ����Ļ���ԭ���ǽ���ͳ��ȼ�������ֱ�ӽӴ���Ӧ��ȼ�ս�����������(��Fe2O3��FeO��)�����÷ֽ�Ϊ�������̷�Ӧ��ȼ�����������Ӵ�,���������������е������ݸ�ȼ�ϡ��ش���������:
(1)��Fe2O3���������Ļ�ѧ��ȼ�ղ����Ȼ�ѧ����ʽ��ѭ��ת����ԭ������:
I.C(s)+H2O(g)==CO(g)+H2(g) ��H1
II.Fe2O3(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) ��H2
III.Fe2O3(s)+1/3H2(g)=2/3Fe3O4(s)+1/3H2O(g) ��H3
IV.Fe3O4(s)+1/4O2(s)=3/2Fe2O3 (s) ��H4
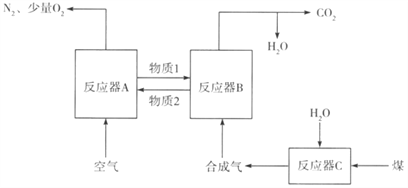
���ڷ�Ӧ��B�н��еķ�Ӧ��_______(�Ӧǰ��Ĵ���)��������2����______(�ѧʽ)��
����ӦC(s)+O2(g)=CO2(g)����H=______(�á�H1����H2����H3����H4��ʾ)��
(2)��FeO�����������ַ�Ӧ��lgKp[Kp����ƽ���ѹ����ƽ��Ũ��(ƽ���ѹ=��ѹ�����ʵ�������)]���¶ȵĹ�ϵ����ͼ��ʾ:
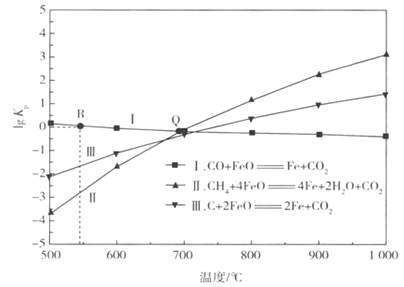
��ͼ���漰�ķ�Ӧ��,�������ȷ�Ӧ����______(�Ӧǰ��Ĵ���)��
�ں����ܱ������н��з�Ӧ:CH4(g) +4FeO(s)=4Fe(s) +2H2O(g)+CO2(g)������˵���÷�Ӧ�Ѵﵽ��ѧƽ��ı�־��______( ����ĸ)��
a.v��(CH4)=v��(CO2)
b.�����ѹǿ������ʱ��仯
c.������ܶȲ�����ʱ��仯
d.��λʱ���ڶ���C-H�������H-O����Ŀ���
����ij�����ܱ�������ֻ������ӦI��II��ƽ��ʱ��Ӧ��ͼ��Q ��ʱ�������������ѹp(X)��Ӧ����Ĺ�ϵ��__________��
����ij�ܱ������г���0.8 molCO��0.2 mol CO2 ������������FeO��ֻ������ӦI����R��(lgKp=0)����CO��ƽ��ת����Ϊ________��
(3)����CaSO4�����������л�ѧ��ȼ��ʱ��CaSO4��CO������Ӧ����CaS����Ӧ�Ļ�ѧ����ʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�����X��Y��Y��Z����ͨ��һ����Ӧ���ת����һ����
ѡ�� | X | Y | Z |
A | Al | NaAlO2(aq) | Al(OH)3 |
B | MgO | MgCl2(aq) | Mg |
C | H2O(g) | Fe3O4 | Fe |
D | NaOH(aq) | Na2CO3(aq) | NaHCO3(aq) |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������(��Ҫ�ɷ�ΪAl2O3����Fe2O3����)Ϊԭ��ұ�����Ĺ����������£�

����������ȷ����
A. �Լ�X����������������Һ��Ҳ����������
B. ��Ӧ�������˺����ó���Ϊ��������
C. ͼ����ʾת����Ӧ������������ԭ��Ӧ
D. ��Ӧ���Ļ�ѧ����ʽΪNaAlO2��CO2��2H2O=Al(OH)3����NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I����һ��������aA��bB![]() cC+dD�ﵽƽ��ʱ������д��
cC+dD�ﵽƽ��ʱ������д��
��1����A��B��C��D�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����a��b��c��d��ϵ��__________________��
��2����֪B��C��D�����壬������A�����ʵ�����ƽ�ⲻ�ƶ���˵��A��__________________����״̬����
��3���������ݻ����䣬��������B������A��ת����__________________����������������С����������������
��4�������Ⱥ�C�İٷֺ�����С��������Ӧ��__________________��Ӧ��������������������������
��5������������ѹǿ���䣬��A��B��C��D�������壬�������г���ϡ�����壬��ѧƽ�������ƶ�����a��b��c��d��ϵ��__________________��
������ҵ��һ��������з�Ӧ�ϳɼ״���CO(g)��2H2(g) ![]() CH3OH(g)��
CH3OH(g)��
��1����һ���¶��£���2 mol CO��6 mol H2����2 L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c(CO)��0.5mol��L��1���÷�Ӧ��ƽ�ⳣ��K��__________________��
��2������һ����ɱ�������г���l molCO�� 2mol H2��1mol CH3OH���ﵽƽ�ⅼ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ��__________________(����������������)��Ӧ�����ƶ���
��3�������¶Ⱥ��ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�˷�Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±���
���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ��(mol/L) | �����仯��Q1��Q2��Q3������0�� |
1 | 2molCO��4molH2 | a1�� | c1 | �ų�Q1kJ���� |
2 | 2molCH3OH | a2�� | c2 | ����Q2kJ���� |
3 | 4molCO��8molH2 | a3�� | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ���� __________________��
A�� c1=c2 B��2Q1=Q3 C��2a1=a3 D��a1 +a2 =1 E���÷�Ӧ������2mol CH3OH����ų�(Q1+Q2)kJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�������������ԭ��Ӧ����
A. 2Na + 2H2O =2NaOH + H2�� B. 2Na + O2![]() Na2O2
Na2O2
C. 2Na2O2 + 2CO2=2Na2CO3+O2 D. NaHCO3+HCl=NaCl+H2O+CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���̣�MnCO3����һ�ָ����ܴ��Բ��ϡ������̿��(��Ҫ��MnO2,������������Fe2O3��Al2O3������)Ϊԭ����ȡMnCO3���������£�

��֪�������̡���ӦΪ��Mn2+ + 2HCO![]() == MnCO3��+ H2O + CO2��
== MnCO3��+ H2O + CO2��
��1���������ʱ��������Ҫ��ӦΪ��2Fe2+ + MnO2+ 4H+ == 2Fe3+ + Mn2+ + 2H2O���������⣬�������ķ�Ӧ���ӷ���ʽΪ________������дһ����
��2�������̡������У�ʵ����MnCO3�IJ�������ҺpH����Ӧʱ��t�Ĺ�ϵ��ͼ��ʾ����ӦҪ����pH��7���ҵ�������_________���������㣩

��3�������ˢ�������Һ�����ʵ���Ҫ�ɷ���_________��
��4��Ϊ�ⶨij���̿��ж������̵�����������ȷ����1.800g���̿���Ʒ������4.020 g������(Na2C2O4)���壬�ټ���������ϡ���Ტ����(���ʲ��μӷ�Ӧ)����ַ�Ӧ����ȴ��������Na2C2O4��0.2000 mol/L���������Һ���еζ���������30.00mL��Һʱǡ����ȫ��Ӧ����֪������ء��������������������¾��ܽ�������(Na2C2O4)������MnO2 + C2O![]() + 4H+
+ 4H+ ![]() Mn2+ + 2CO2��+ 2H2O��MnO4��+ C2O
Mn2+ + 2CO2��+ 2H2O��MnO4��+ C2O![]() + H+ �� Mn2+ + CO2��+ H2O ��δ��ƽ����������̿��ж������̵���������_________(д���������)��
+ H+ �� Mn2+ + CO2��+ H2O ��δ��ƽ����������̿��ж������̵���������_________(д���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д�����۾���������( )
ѡ�� | ���ӷ���ʽ | ���� |
A | ��2 mol Cl2ͨ�뺬1 mol FeI2����Һ�У� 2Fe2����2I����2Cl2===2Fe3����4Cl����I2 | ��ȷ��Cl2�������ɽ�Fe2����I�������� |
B | Ba(HCO3)2��Һ��������NaOH��Һ��Ӧ�� Ba2����HCO3-��OH��===BaCO3����H2O | ��ȷ����ʽ����Ӧ�������κ�ˮ |
C | ����SO2ͨ��NaClO��Һ�У� SO2��H2O��ClO��===HClO��HSO3- | ��ȷ��˵�����ԣ�H2SO3ǿ��HClO |
D | 1 mol/L��NaAlO2��Һ��2.5 mol/L��HCl��Һ�������ϣ� 2AlO2-��5H��===Al3����Al(OH)3����H2O | ��ȷ����һ����Ӧ�͵ڶ�����Ӧ���ĵ�H�������ʵ���֮��Ϊ2��3 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com