
【题目】在密闭容器 中发生反应 aA(g) +bB(s) ![]() cC(g)+dD(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,D 的浓度为原平衡的 1.7 倍,下列判断正确的是()
cC(g)+dD(g),反应达到平衡后,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时,D 的浓度为原平衡的 1.7 倍,下列判断正确的是()
A. a+b < c+d B. D 的物质的量增加
C. A 的转化率变小 D. 平衡向正反应方向移动
科目:高中化学 来源: 题型:
【题目】25℃时,在25 mL 0.1mol/L的NaOH溶液中,逐滴加入0.2 mol/L的CH3COOH溶液,液pH与CH3COOH溶液体积关系如下图所示,下列有关粒子浓度大小关系正确的是
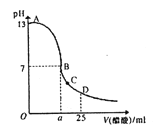
A. a=12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
B. C点时溶液中有: c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C. D点时溶液中有: c(CH3COO-) + c(CH3COOH)=2c (Na+)
D. 曲线上A、B间的任意一点,溶液中都有: c(Na+)>c(CH3COO-) >c(H+) >c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。
(1)己知: N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1
2C(S)+O2(g)=2CO(g) △H=-221kJ·mol-1
若某反应的平衡常数表达式c(N2)·c2(CO2)/ c(NO)·c2(CO)为: 请写出此反应的热化学方程式______________。
(2)利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)
CH2=CH2(g)+4H2O(g)
己知不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法正确的是_____(填序号)。
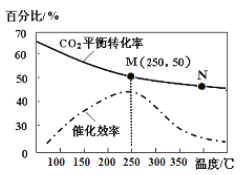
①不同条件下反应,N点的速率最大
②N点时平衡常数比M点时平衡常数小
③温度低于250℃时,随温度升高乙烯的产率增大
④实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(2)在密闭容器中充入5molCO和4molNO,发生上述(1)中某反应,如图为平衡时NO的体积分数与温度,压强的关系。
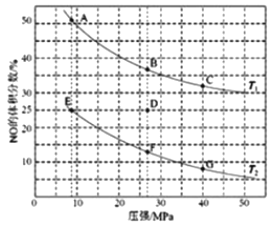
回答下列问题:
①温度:T1_______T2(填“<“ 或“>”)。
②某温度下,若反应进行到10 分钟达到平衡状态D点时,容器的体积为2L,则此时的平衡常数K=___(结果精确到两位小数);用CO的浓度变化表示的平均反应速率V(CO)=_______。
③若在D点对反应容器降温的同时扩大体积至体系压强减小,重新达到的平衡状态可能是图中A~G点中的______点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要化工原料,其产量是一个国家石油化工水平的标志.通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品.已知乙烯能发生如图转化: 
(1)乙烯的结构简式为 .
(2)反应①的反应类型是 , D中含官能团名称为 .
(3)写出以下反应的化学方程式:①;②;③ .
(4)乙烯大量用来生产环氧乙烷,生产工艺主要有两种:
工艺一: ![]()
工艺二: ![]()
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,在实际生产中,应采用(填“工艺一”或“工艺二”)更环保、更经济.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,99 ml 0.1 mol/L盐酸和101 ml 0.05 mol/L氢氧化钡溶液相混和(忽略混合后溶液的体积变化),则混合后溶液的pH值为( )
A. 1.7 B. 10.7 C. 11 D. 11.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是____和____(填分子式)。
(2)已知①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=+206.1kJ·mol–1
则反应CH4(g)=C(s)+2H2(g)的ΔH=_______________kJ·mol–1
(3)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。
pH t /min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
50 | 31 | 26 | 15 | 7 |
①pH增大能加速O3分解,表明对O3分解起催化作用的微粒是____。
②在30 ℃、pH=4.0条件下,O3的分解速率为_____mol/(L·min)。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为_____(填字母)。
a.40 ℃、pH=3.0 b.10 ℃、pH=4.0 c.30 ℃、pH=7.0
(4)O3可由臭氧发生器(原理如图)电解稀硫酸制得。
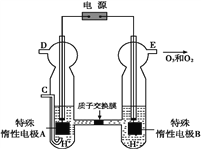
①图中阴极为____(填“A”或“B”),其电极反应式为_________________________。
②若C处通入O2,则A极的电极反应式为________,右室pH变化___________(填升高、降低、不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.01mol的铁、铝混合物溶于100mL 0.2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示.当V1=16mL时,则V2为( ) 
A.24mL
B.30mL
C.440mL
D.44mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeCl3、CuCl2、盐酸的混合溶液中加入铁粉充分反应后,用KSCN溶液检验无明显现象,则反应后的溶液一定
A.含Cu2+B.含Fe2+C.呈中性D.含Fe2+和Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com